Priorix, injektiokuiva-aine ja liuotin, liuosta varten esitäytetyssä ruiskussa
Tuhkarokko-sikotauti-vihurirokkorokote, elävä
Yleisiä ohjeita
Lue tämä pakkausseloste huolellisesti ennen kuin saat tätä rokotetta, sillä se sisältää sinulle tärkeitä tietoja.
- Säilytä tämä pakkausseloste. Voit tarvita sitä myöhemmin.
- Jos sinulla on kysyttävää, käänny lääkärin tai apteekkihenkilökunnan puoleen.
- Tämä rokote on määrätty vain sinulle, eikä sitä tule antaa muiden käyttöön.
- Jos havaitset haittavaikutuksia, kerro niistä lääkärille tai apteekkihenkilökunnalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Ks. kohta Mahdolliset haittavaikutukset.
Tämä pakkausseloste on laadittu rokotetta saavalle henkilölle. Rokote voidaan kuitenkin antaa sekä aikuisille että lapsille, joten viittaus sinuun voi myös tarkoittaa lastasi.
Tässä pakkausselosteessa kerrotaan
- Mitä Priorix on ja mihin sitä käytetään
- Mitä sinun on tiedettävä, ennen kuin saat Priorixia
- Miten Priorix annetaan
- Mahdolliset haittavaikutukset
- Priorixin säilyttäminen
- Pakkauksen sisältö ja muuta tietoa
1. Mitä valmiste on ja mihin sitä käytetään
Priorix on rokote, jota käytetään 9 kuukauden iästä lähtien lapsilla, nuorilla ja aikuisilla suojaamaan tuhkarokko-, sikotauti- ja vihurirokkovirusten aiheuttamia tauteja vastaan.
Miten Priorix vaikuttaa
Priorix-rokotus saa elimistön immuunijärjestelmän tuottamaan suojaavia vasta-aineita tuhkarokko-, sikotauti-, ja vihurirokkovirusten aiheuttamia infektioita vastaan. Immuunijärjestelmä on elimistön luonnollinen puolustusjärjestelmä.
Priorixin sisältämät elävät virukset ovat liian heikkoja aiheuttamaan tuhkarokkoa, sikotautia tai vihurirokkoa terveillä henkilöillä.
2. Mitä sinun on tiedettävä ennen valmisteen käyttöä
Priorixia ei saa antaa, jos
- sinulla on aiemmin esiintynyt allerginen reaktio tämän rokotteen jollekin muulle aineelle (lueteltu kohdassa Pakkauksen sisältö ja muuta tietoa). Allergisen reaktion merkkejä voivat olla kutiseva ihottuma, hengenahdistus ja kasvojen tai kielen turpoaminen.
- sinulla on todettu neomysiiniallergia (antibiootti). Aikaisemman kosketusihottuman (ihottuma syntyy, kun iho on suorassa kosketuksessa neomysiiniallergeenin kanssa) ei pitäisi olla ongelma, mutta neuvottele ensin lääkärin kanssa.
- sinulla on vaikea kuumeinen infektio. Tällöin on syytä siirtää rokotusta myöhemmäksi, kunnes sinä olet toipunut. Vähäisen infektion, kuten nuhakuumeen, ei pitäisi aiheuttaa ongelmaa, mutta keskustele asiasta ensin lääkärin kanssa.
- sinä sairastat tautia, joka heikentää vastustuskykyä (kuten HIV-tartunta eli immuunikatovirustartunta tai AIDS (immuunikatotauti)), tai jos sinä otat lääkettä, joka heikentää vastustuskykyä. Immuunikatotilan vaikeus ratkaisee, saatko sinä rokotetta.
- olet raskaana. Raskautta on lisäksi vältettävä 1 kuukausi rokotuksen jälkeen.
Varoitukset ja varotoimet
Keskustele lääkärin tai apteekkihenkilökunnan kanssa ennen kuin saat Priorixia, jos
- sinulla on jokin keskushermostosairaus tai jos sinulla on ollut aikaisemmin kuumekouristuksia tai jos perheessä on esiintynyt kouristuksia. Ota heti yhteys lääkäriin, jos rokotus aiheuttaa korkeaa kuumetta.
- kananmunan proteiini on joskus aiheuttanut sinulle vaikean allergisen reaktion.
- aikaisempi tuhkarokko-, sikotauti- tai vihurirokkorokotus on aiheuttanut haittavaikutuksena mustelmataipumusta tai epätavallisen pitkään jatkunutta verenvuotoa (ks. kohta Mahdolliset haittavaikutukset).
- sinulla on heikentynyt vastustuskyky (esim. HIV-tartunta). Sinua tai lastasi seurataan huolellisesti, sillä rokotteen aikaansaama vaste ja suoja tautia vastaan saattaa jäädä puutteelliseksi (ks. kohta Mitä sinun on tiedettävä ennen valmisteen käyttöä ”Priorixia ei saa antaa”).
Pyörtymistä voi esiintyä (enimmäkseen nuorilla) pistoksena annettavan rokotuksen jälkeen, tai jopa ennen. Kerro lääkärille tai hoitajalle, jos olet pyörtynyt aikaisemman pistoksena annettavan rokotuksen yhteydessä.
Priorix suojaa jossain määrin sinua, jos rokotus annetaan 72 tunnin sisällä tuhkarokkoaltistuksesta.
Alle 12 kuukauden ikäiset lapset
Ensimmäisenä ikävuotena annettu rokotus ei ehkä anna täyttä suojaa. Lääkäri kertoo mahdollisten lisäannosten tarpeesta.
Kuten muutkin rokotteet, Priorix ei ehkä täysin suojaa kaikkia rokotettuja.
Muut lääkevalmisteet ja Priorix
Kerro lääkärillesi, jos parhaillaan saat tai jos olet äskettäin saanut tai jos saatat joutua saamaan muita lääkkeitä tai jos sinä olet äskettäin saanut jonkin muun rokotuksen.
Priorix voidaan antaa samanaikaisesti muiden rokotteiden kanssa: kurkkumätä-, jäykkäkouristus-, soluton hinkuyskärokote, Haemophilus influenzae tyyppi b -rokote, suun kautta otettava tai inaktivoitu poliorokote, hepatiitti A- ja B-rokote, vesirokko-, meningokokki seroryhmä B -rokotteet, kuin myös meningokokki seroryhmä C -rokotteet, meningokokki seroryhmät A-, C-, W-135- ja Y-rokotteet sekä konjugoitu pneumokokkirokote. Kysy lisätietoja lääkäriltä tai sairaanhoitajalta. Jokainen rokotus tulee antaa eri injektiokohtaan.
Ellei muita eläviä heikennettyjä rokotteita anneta samanaikaisesti, rokotusten välillä on oltava vähintään yksi kuukausi.
Lääkäri voi lykätä rokotusta vähintään 3 kuukautta, jos sinulle on annettu verensiirto tai ihmisen immunoglobuliineja.
Mikäli tuberkuliinikoe aiotaan tehdä, se olisi tehtävä ennen Priorix-rokotusta, rokotuksen yhteydessä tai 6 viikkoa rokotuksen jälkeen.
Raskaus, imetys ja hedelmällisyys
Priorixia ei saa antaa raskaana oleville naisille.
Jos olet raskaana tai imetät, epäilet olevasi raskaana tai jos suunnittelet lapsen hankkimista, kysy lääkäriltä tai apteekkihenkilökunnalta neuvoa ennen kuin rokotus annetaan. On myös tärkeää, että et tule raskaaksi kuukauden sisällä rokotuksesta. Tänä aikana sinun on käytettävä tehokasta ehkäisyä raskauden välttämiseksi.
Tahaton rokotus Priorixilla raskaana olevalle naiselle ei ole raskauden keskeytyksen peruste.
Priorix sisältää sorbitolia, para-aminobentsoehappoa, fenyylialaniinia, natriumia ja kaliumia
Tämä rokote sisältää 9 mg sorbitolia per annos.
Priorix sisältää para-aminobentsoehappoa. Saattaa aiheuttaa allergisia reaktioita (mahdollisesti viivästyneitä) ja poikkeustapauksissa bronkospasmia. Tämä rokote sisältää 334 mikrogrammaa fenyylialaniinia per annos. Fenyylialaniini voi olla haitallista, jos sinulla on fenyyliketonuria (PKU), harvinainen perinnöllinen sairaus, jossa kertyy fenyylialaniinia, koska elimistö ei kykene poistamaan sitä kunnolla
Tämä rokote sisältää alle 1 mmol natriumia (23 mg) per annos eli sen voidaan sanoa olevan ”natriumiton”. Tämä rokote sisältää kaliumia alle 1 mmol (39 mg) per annos eli sen voidaan sanoa olevan ”kaliumiton”.
3. Miten valmistetta käytetään
Priorix annetaan ihon alle tai lihakseen, joko olkavarteen tai ulkoreiteen.
Priorix on tarkoitettu 9 kuukauden iästä lähtien lapsille, nuorille ja aikuisille.
Lääkäri määrää asianmukaisia virallisia suosituksia noudattaen, montako rokotusta sinulle annetaan ja niiden ajankohdan.
Rokotetta ei saa milloinkaan antaa suoneen.
4. Mahdolliset haittavaikutukset
Kuten kaikki lääkkeet, tämäkin lääke voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa.
Kliinisissä tutkimuksissa Priorixilla on esiintynyt seuraavia haittavaikutuksia:
Hyvin yleiset (ilmaantuvat 1 rokoteannoksella 10:stä tai useammin):
- punoitus injektiokohdassa
- korkea kuume (38 ºC tai sitä korkeampi).
Yleiset (ilmaantuvat harvemmin kuin 1 rokoteannoksella 10:stä):
- kipu ja turvotus injektiokohdassa
- kuume (39,5 ºC tai sitä korkeampi)
- ihottuma (läikkiä)
- ylähengitystieinfektiot.
Melko harvinaiset (ilmaantuvat harvemmin kuin 1 rokoteannoksella 100:sta):
- välikorvan tulehdus
- imusolmukkeiden turpoaminen niskassa, kainalokuopassa tai nivusissa
- ruokahaluttomuus
- hermostuneisuus
- epätavallinen itku
- unettomuus (insomnia)
- silmien punoitusta, ärtyneisyyttä ja vetisyyttä (konjunktiviitti)
- keuhkoputkentulehdus
- yskä
- korvasylkirauhasen turpoaminen (poskissa)
- ripuli
- oksentelu.
Harvinaiset (ilmaantuvat harvemmin kuin 1 rokoteannoksella 1000:sta):
- kouristukset, joihin liittyy korkea kuume
- allergiset reaktiot.
Markkinoille tulon jälkeen Priorixilla on raportoitu satunnaisesti seuraavia haittavaikutuksia:
- nivel- ja lihaskipu
- pistemäisiä tai pieniä verenvuotoja tai mustelmataipumusta. Tämä johtuu verihiutaleiden määrän laskusta.
- äkilliset henkeä uhkaavat allergiset reaktiot
- aivojen, selkäytimen ja ääreishermoston tulehdus tai infektio, mikä johtaa tilapäisiin kävelyvaikeuksiin (tasapainohäiriöihin) ja/tai tilapäiseen vaikeuteen kontrolloida liikkeitä, joidenkin hermojen tulehdus, johon voi liittyä pistelyä ja puutumista tai normaalin liikkeen tuntohäiriötä (Guillan-Barrén oireyhtymä)
- verisuonten ahtauma tai tukos
- erythema multiforme (oireena punaiset, kutisevat läiskät, jotka muistuttavat tuhkarokkoa. Läiskät ilmaantuvat ensin raajoissa ja joskus kasvoissa ja koko kehossa.)
- tuhkarokkoa ja sikotautia muistuttavat oireet (mukaan lukien ohimenevä, kivulias kivesten turpoaminen ja kaularauhasten turpoaminen).
Haittavaikutuksista ilmoittaminen
Jos havaitset haittavaikutuksia, kerro niistä lääkärille tai apteekkihenkilökunnalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Voit ilmoittaa haittavaikutuksista myös suoraan (ks. yhteystiedot alla). Ilmoittamalla haittavaikutuksista voit auttaa saamaan enemmän tietoa tämän lääkevalmisteen turvallisuudesta.
www-sivusto: www.fimea.fi
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
00034 FIMEA
5. Valmisteen säilyttäminen
Ei lasten ulottuville eikä näkyville.
Älä käytä tätä lääkettä pakkauksessa mainitun viimeisen käyttöpäivämäärän jälkeen (EXP).
Viimeinen käyttöpäivämäärä tarkoittaa kuukauden viimeistä päivää.
Säilytä ja kuljeta kylmässä (2 °C – 8 °C).
Ei saa jäätyä.
Säilytä alkuperäispakkauksessa. Herkkä valolle.
Rokote on annettava nopeasti sekoittamisen jälkeen. Jos tämä ei ole mahdollista, rokote on säilytettävä jääkaapissa (2 °C – 8 °C:ssa) ja käytettävä 8 tunnin sisällä sekoittamisesta.
Lääkkeitä ei tule heittää viemäriin eikä hävittää talousjätteiden mukana. Kysy käyttämättömien lääkkeiden hävittämisestä apteekista. Näin menetellen suojelet luontoa.
6. Pakkauksen sisältö ja muuta tietoa
Mitä Priorix sisältää
Vaikuttavat aineet ovat:
Eläviä heikennettyjä tuhkarokko-, sikotauti- ja vihurirokkoviruksia.
Muut aineet ovat:
Injektiokuiva-aine: Aminohapot (sisältää fenyylialaniinia), laktoosi (vedetön), mannitoli (E 421), sorbitoli (E 420), medium 199 (sisältää fenyylialaniinia, para-aminobentsoehappoa, natriumia ja kaliumia).
Liuotin: Injektionesteisiin käytettävä vesi.
Lääkevalmisteen kuvaus ja pakkauskoko
Priorixia on saatavana injektiokuiva-aineena ja liuottimena, liuosta varten, esitäytetyssä ruiskussa. (Injektiokuiva-aine on 1 annoksen injektiopullossa ja liuotin on esitäytetyssä ruiskussa (0,5 ml) neuloilla tai ilman neuloja). Pakkauskoot ovat:
- kahdella erillisellä neulalla: pakkauskoot 1 tai 10
- ilman neulaa: pakkauskoot 1 tai 10
Priorix on valkoinen tai hieman punertava jauhe ja liuotin on kirkas ja väritön (injektionesteisiin käytettävää vettä). Jauhe liuotetaan liuottimeen.
Kaikkia pakkauskokoja ei välttämättä ole kaupan.
Myyntiluvan haltija ja valmistaja
GlaxoSmithKline Biologicals s.a.
Rue de l'Institut 89
B-1330 Rixensart
Belgia
Lisätietoja tästä lääkevalmisteesta antaa myyntiluvan haltijan paikallinen edustaja.
GlaxoSmithKline Oy
Porkkalankatu 20 A
00180 Helsinki
Puh: + 358 10 30 30 30
Tämä pakkausseloste on tarkistettu viimeksi 6.9.2023
Muut tiedonlähteet
Lisätietoa tästä lääkevalmisteesta on saatavilla www.fimea.fi verkkosivulla.
Ohjeet terveydenhuollon ammattilaiselle
Kuten yleensäkin, kun rokotus annetaan injektiona, potilasta on seurattava harvinaisten anafylaktisten reaktioiden varalta rokotuksen jälkeen ja asianmukaisesta hoitovalmiudesta on huolehdittava.
Alkoholin ja muiden desinfektioaineiden on annettava haihtua iholta ennen injektiota, jotta rokotteen sisältämät heikennetyt virukset eivät inaktivoituisi.
Priorixia ei saa missään olosuhteissa antaa suoneen.
Yhteensopivuustutkimusten puuttuessa tätä lääkettä ei pidä sekoittaa muiden lääkkeiden kanssa.
Liuotin ja käyttökuntoon saatettu rokote on tarkastettava silmämääräisesti ennen käyttökuntoon saattamista ja antamista mahdollisten vierasainehiukkasten ja/tai fysikaalisten ominaisuuksien muutosten havaitsemiseksi. Mikäli tällaisia muutoksia havaitaan, liuotinta tai käyttökuntoon saatettua rokotetta ei saa käyttää.
Rokote saatetaan käyttökuntoon lisäämällä liuotinta sisältävän esitäytetyn ruiskun koko sisältö injektiokuiva-ainetta sisältävään injektiopulloon.
Lue huolellisesti ohjeet sekä kuvat 1 ja 2 neulan kiinnittämisestä ruiskuun. Priorix-pakkauksessa oleva ruisku voi hieman poiketa (ilman kierreosaa) kuvassa olevasta ruiskusta. Tällöin neula on kiinnitettävä ilman kiertoliikettä.
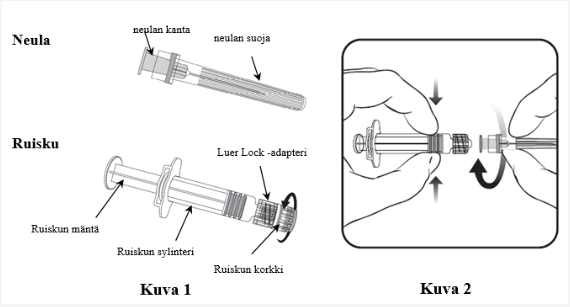
Pidä aina ruiskun sylinteristä kiinni, älä pidä kiinni ruiskun männästä tai Luer Lock -adapterista (LLA). Pidä neula samassa linjassa ruiskun kanssa (kuten kuvassa 2). Jos tätä ei tehdä, LLA saattaa vääntyä ja vuotaa.
Jos LLA irtoaa ruiskun kokoamisen aikana, tulee käyttää uutta rokotetta (uusi ruisku ja injektiopullo).
1. Poista ruiskun korkki kiertämällä vastapäivään (kuten kuvassa 1).
Seuraa seuraavia ohjeita riippumatta siitä pyöriikö LLA vai ei:
2. Kiinnitä neula ruiskuun yhdistämällä kevyesti neulan kanta LLA:iin ja kääntämällä neljäsosakierroksen myötäpäivään, kunnes neula tuntuu lukkiutuvan (kuten kuvassa 2).
3. Poista neulan suoja, joka voi tuntua jäykältä.
4. Lisää liuotin injektiokuiva-aineeseen. Seosta on ravistettava, kunnes injektiokuiva-aine on täysin liuennut liuottimeen.
Vähäisten pH-muutosten vuoksi käyttökuntoon saatetun rokotteen väri voi vaihdella kirkkaan persikanvärisestä fuksian vaaleanpunaiseen. Tämä ei vaikuta rokotteen tehoon.
5. Koko injektiopullon sisältö vedetään ruiskuun.
6. Käytä toista neulaa rokotteen antamiseen. Poista neula ruiskusta ja kiinnitä injektointiin käytettävä neula toistamalla yllä oleva kohta Mitä sinun on tiedettävä ennen valmisteen käyttöä.
Käyttökuntoon saattamisen jälkeen rokote tulee antaa nopeasti. Jos tämä ei ole mahdollista, rokote on säilytettävä jääkaapissa (2 °C – 8 °C:ssa) ja käytettävä 8 tunnin sisällä sekoittamisesta.
Käyttämätön lääkevalmiste tai jäte on hävitettävä paikallisten vaatimusten mukaisesti.