Glycostigmin®-injektionsvätska, lösning
neostigminmetylsulfat och glykopyrroniumbromid
Allmänna direktiv
Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig.
- Spara denna information, du kan behöva läsa den igen.
- Om du har ytterligare frågor vänd dig till läkare eller apotekspersonal.
- Detta läkemedel har ordinerats enbart åt dig. Ge det inte till andra. Det kan skada dem, även om de uppvisar sjukdomstecken som liknar dina.
- Om du får biverkningar, tala med läkare eller apotekspersonal. Detta gäller även eventuella biverkningar som inte nämns i denna information. Se avsnitt Eventuella biverkningar.
I denna bipacksedel finns information om följande
1. Vad Glycostigmin är och vad det används för
2. Vad du behöver veta innan du använder Glycostigmin
3. Hur du använder Glycostigmin
4. Eventuella biverkningar
5. Hur Glycostigmin ska förvaras
6. Förpackningens innehåll och övriga upplysningar
1. Vad produkten är och vad den används för
1 ml injektionsvätska innehåller 2,5 mg neostigminmetylsulfat och 0,5 mg glykopyrroniumbromid.
Preparatet används vid upphävning av neuromuskulär residual blockad orsakad av kompetitiv nondepolariserande muskelrelaxant.
Neostigminmetylsulfat och glykopyrroniumbromid som finns i Glycostigmin-injektionsvätska kan också vara godkänd för att behandla andra sjukdomar som inte nämns i denna produktinformation. Fråga läkare, apotek eller annan hälsovårdspersonal om du har ytterligare frågor och följ alltid deras instruktion.
2. Vad du behöver veta innan produkten används
Använd inte Glycostigmin
- om patienten är allergisk mot neostigminmetylsulfat eller glykopyrroniumbromid eller något annat innehållsämne i detta läkemedel (anges i avsnitt Förpackningens innehåll och övriga upplysningar)
- om patienten har en mekanisk obstruktion i mag-tarmkanalen eller urinvägarna
- om muskelrelaxation är orsakad av suxameton.
Varningar och försiktighet
Glycostigmin-injektionsvätska skall ges med försiktighet till patienter som har någon hjärtsjukdom såsom kranskärlssjukdom, hjärtinsufficiens eller rytmrubbningar.
Glycostigmin skall användas med försiktighet också om patienten lider av blodtryckssjukdom, tyreotoxikos, epilepsi, Parkinsons sjukdom, hög feber, astma, benägenhet för bronkospasm eller betydande bradykardi. Glykopyrrolat skall ges med försiktighet till patienter med glaucoma congestivum, prostatahyperplasi eller någon annan sjukdom som medför urinretention.
Glycostigmin skall ges för upphävning av muskelrelaxation först när den neuromuskulära blockaden redan börjar avmattas. Om relaxationen upphävs under en total neuromuskulär blockad, kan patienten drabbas av så kallad efterrelaxation.
Andra läkemedel och Glycostigmin
Tala om för läkare eller apotekspersonal om du tar, nyligen har tagit eller kan tänkas ta andra läkemedel.
Neostigminmetylsulfat förstärker neuromuskulär blockad orsakad av suxameton och Glycostigmin skall därför inte användas i samband med muskelrelaxation orsakad av suxameton.
Vissa läkemedel, såsom tricykliska depressionsmediciner, neuroleptika och vissa antihistaminer, kan förstärka glykopyrrolatets antikolinerga effekt.
Graviditet och amning
Glykopyrrolat och neostigminmetylsulfat har inte undersökts med avseende på säkerhet under graviditet och amning. Eftersom föreningarna tränger dåligt igenom biologiska hinnor passerar efter en engångsdos endast en ringa mängd genom moderkakan eller över till modersmjölken. Vid terapeutiska doser utsätts därför fostret eller den nyfödda sannolikt inte för någon betydande risk.
Körförmåga och användning av maskiner
Preparatets inverkan på körförmågan och förmågan att använda maskiner har inte undersökts.
Du är själv ansvarig för att bedöma om du är i kondition att framföra motorfordon eller utföra arbeten som kräver skärpt uppmärksamhet. En av faktorerna som kan påverka din förmåga i dessa avseenden är användning av läkemedel på grund av deras effekter och/eller biverkningar. Beskrivning av dessa effekter och biverkningar finns i andra avsnitt. Läs därför all information i denna bipacksedel för vägledning. Diskutera med din läkare eller apotekspersonal om du är osäker.
Glycostigmin innehåller natrium
Detta läkemedel innehåller mindre än 1 mmol (23 mg) natrium per 1 ml ampull, d.v.s. är näst intill “natriumfritt”.
3. Hur produkten används
Använd alltid detta läkemedel enligt läkarens anvisningar. Rådfråga läkare om du är osäker.
Dosering
Vuxna och åldringar
1,25–5 mg neostigminmetylsulfat och 0,25–1 mg glykopyrrolat (= 0,5–2 ml Glycostigmin) intravenöst under 10–30 sekunder. Om Glycostigmin-dosen räknas i milliliter per kilo kroppsvikt, kan under 10–30 sekunder alltså injiceras 0,01–0,02 ml/kg.
Barn
0,02 ml/kg intravenöst under 10–30 sekunder (50 mikrog/kg neostigminmetylsulfat och 10 mikrog/kg glykopyrrolat).
Dosen kan vid behov upprepas, om den neuromuskulära blockaden inte upphävs tillräckligt effektivt. Den maximala Glycostigmin-dosen är dock totalt 2 ml.
Om du har fått för stor mängd av Glycostigmin
Om du har fått I dig för stor mängd läkemedel eller om t.ex. ett barn fått i sig läkemedlet av misstag kontakta läkare, sjukhus eller Giftinformationscentralen (tel. 0800 147 111) för bedömning av risken samt rådgivning.
Behandlingen av överdosering beror på om de dominerande symptomen härrör sig från en överdosering av antikolinesteras eller en antikolinerg förening.
En överdosering av neostigminmetylsulfat ger sig till känna framför allt i form av symptom av samma typ som muskarineffekt, dvs. ökad utsöndring av sekret i luftvägarna och mag-tarmkanalen, bronkospasm, magkramper, bradykardi och rytmrubbningar i hjärtat. Dessa kan behandlas med glykopyrrolat (0,2–0,6 mg/kg i.v.) eller atropin (0,5–1,0 mg i.v.). I nödsituationer är det skäl att komma ihåg att atropin verkar snabbare. Eventuell andningsinsufficiens skall vid behov åtgärdas mekaniskt.
Symptom på överdosering av glykopyrrolat (takykardi, kammarextraslag och övriga rytmrubbningar) kan behandlas genom att man ger samma mängd neostigmin (= 1 mg neostigminmetylsulfat per en 1 mg glykopyrrolatdos). Eftersom symptomen på överdoseringen av glykopyrrolat är huvudsakligen perifera, är det i allmänhet inte nödvändigt att använda fysostigmin.
4. Eventuella biverkningar
Liksom alla läkemedel kan detta läkemedel orsaka biverkningar, men alla användare behöver inte få dem.
Biverkningarna av neostigminmetylsulfat och glykopyrrolat beror närmast på föreningarnas farmakologiska verkningar och är delvis motsatta.
Neostigminmetylsulfat kan orsaka ökad utsöndring av sekret i munnen, svalget och andningsvägarna, rytmrubbningar i hjärtat, särskilt bradykardi, samt försnabbning av mag-tarmkanalens funktion. De vanligaste biverkningarna av glykopyrrolat är torrhet i mun och svalg, synrubbningar, funktionsstörningar i ögats adaptionsmuskel, urineringssvårigheter, olika typer av rytmrubbningar såsom takykardi och palpitation, samt förhindrad transpiration.
Rapportering av biverkningar
Om du får biverkningar, tala med läkare, apotekspersonal eller sjuksköterska. Detta gäller även biverkningar som inte nämns i denna information. Du kan också rapportera biverkningar direct (se kontaktuppgifter nedan). Geno matt rapportera biverkningar kan du bidra till att öka informationen om läkemedlets säkerhet.
webbplats: www.fimea.fi
Säkerhets- och utvecklingscentralen för läkemedelsområdet Fimea
Biverkningsregistret
PB 55
00034 FIMEA
5. Hur produkten ska förvaras
Förvara detta läkemedel utom syn- och räckhåll för barn.
Förvaras vid högst 25 °C. Förvara ampullen i ytterförpackningen. Ljuskänsligt.
Används före utgångsdatum som anges på förpackningen. Utgångsdatumet är den sista dagen i angiven månad.
Använd inte detta läkemedelom det synbart har förändrats.
Läkemedel ska inte kastas i avloppet eller bland hushållsavfall. Fråga apotekspersonalen hur man kastar läkemedel som inte längre används. Dessa åtgärder är till för att skydda miljön.
6. Förpackningens innehåll och övriga upplysningar
Innehållsdeklaration
- De aktiva substanserna är neostigminmetylsulfat och glykopyrroniumbromid
- Övriga innehållsämnen är dinatriumfosfatdihydrat, citronsyramonohydrat, vatten för injektionsvätskor.
Läkemedlets utseende och förpackningsstorlekar
Klar, färglös lösning
10 x 1 ml, 25 x 1 ml och 50 x 1 ml, ofärgad, sluten ampull av glas, en grön ring runt ampullens hals.
Eventuellt kommer inte alla förpackningsstorlekar att marknadsföras.
Innehavare av godkännande för försäljning
Takeda Oy, PB 1406, 00101 Helsingfors, tel. 020 746 5000
Tillverkare
Takeda Austria GmbH, St. Peter Strasse 25 och 4020 Linz, Österrike
Bipacksedeln är granskad 4.3.2020
-------------------------------------------------------------------------------------------
Direktiv för experterna inom hälsovården
Ampullerna med Glycostigmin-injektionsvätska är s.k. One-Point-Cut-ampuller (OPC) som ska öppnas genom att de bryts av för hand utan fil eller andra hjälpmedel. På ampullens spets finns en punkt som man ska trycka på då man öppnar ampullen.
Då ampullen öppnas enligt följande anvisning, hamnar det inga glasskärvor eller färgämnen från färgringarna i lösningen. Anvisningen är avsedd för högerhänta personer.
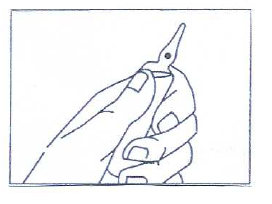
FAS 1:
Håll ampullen i vänstra handen med nedre delen mellan tummen och pekfingret och fingrarna strax under ampullens hals. Kläm inte åt för hårt. Håll ampullen med spetsen mot dig själv.
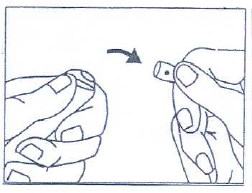
FAS 2:
Ta tag i ampullens övre del med högra tummen och pekfingret så att tummen täcker hela övre delen.
FAS 3:
Tryck den övre delen från dig själv med högra tummen och håll emot med vänstra pekfingret på den nedre delen. Dra eller skruva inte på ampullen (rör inte händerna i motsatt riktning eller närmare varandra). Använd inte för mycket kraft utan tryck jämnt för att bryta av ampullens hals.