Prostivas 0,5 mg/ml infuusiokonsentraatti, liuosta varten
alprostadiili
Yleisiä ohjeita
Lue tämä pakkausseloste huolellisesti, ennen kuin aloitat lääkkeen käyttämisen, sillä se sisältää sinulle tärkeitä tietoja.
- Säilytä tämä pakkausseloste. Voit tarvita sitä myöhemmin.
- Jos sinulla on kysyttävää, käänny lääkärin, apteekkihenkilökunnan tai sairaanhoitajan puoleen.
- Tämä lääke on määrätty vain sinulle eikä sitä tule antaa muiden käyttöön. Se voi aiheuttaa haittaa muille, vaikka heillä olisikin samanlaiset oireet kuin sinulla.
- Jos havaitset haittavaikutuksia, käänny lääkärin, apteekkihenkilökunnan tai sairaanhoitajan puoleen. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Ks. kohta Mahdolliset haittavaikutukset.
Tässä pakkausselosteessa kerrotaan
1. Mitä Prostivas on ja mihin sitä käytetään
2. Mitä sinun on tiedettävä, ennen kuin käytät Prostivas-valmistetta
3. Miten Prostivas-valmistetta käytetään
4. Mahdolliset haittavaikutukset
5. Prostivas-valmisteen säilyttäminen
6. Pakkauksen sisältö ja muuta tietoa
1. Mitä valmiste on ja mihin sitä käytetään
Alprostadiili on tarkoitettu oireita lievittäväksi, ei parantavaksi hoidoksi vastasyntyneille, joilla on synnynnäinen sydänvika ja joiden eloonjääminen riippuu valtimotiehyen (ductus arteriosus) avoimena pysymisestä. Alprostadiili pitää valtimotiehyen tilapäisesti avoimena, kunnes lapselle voidaan tehdä korjaava tai oireita lievittävä toimenpide.
Tällaisia synnynnäisiä sydänvikoja ovat esimerkiksi hiippaläpän atresia, keuhkovaltimoläpän atresia, keuhkovaltimoläpän ahtauma, trikuspidaaliläpän atresia, Fallot´n tetralogia, aortan kaaren kehityshäiriö, aortan ahtauma tai suurten valtasuonten virhesijainti, johon saattaa liittyä myös muita vikoja.
2. Mitä sinun on tiedettävä ennen valmisteen käyttöä
Älä käytä Prostivas-valmistetta
- jos lapsi on allerginen (yliherkkä) alprostadiilille tai Prostivas-valmisteen jollekin muulle aineelle
- jos lapsella on hyaliinimembraanitauti (respiratory distress -oireyhtymä, RDS).
Varoitukset ja varotoimet
Keskustelelääkärin, apteekkihenkilökunnan tai sairaanhoitajan kanssa, ennen kuin käytät Prostivas-valmistetta
- jos lapsella on taipumus saada hengityskatkoksia (apnea). Apneaa ilmenee noin 10 - 12 prosentilla niistä synnynnäistä sydänvikaa sairastavista vastasyntyneistä, jotka saavat alprostadiilia. Apneaa ilmenee useimmiten vastasyntyneillä, joiden syntymäpaino on alle 2 kg, ja se alkaa yleensä ensimmäisen tunnin kuluessa infuusion aloittamisesta.
Muut lääkevalmisteet ja Prostivas
Kerro lääkärille tai apteekkihenkilökunnalle, jos lapsesi parhaillaan käyttää tai on äskettäin käyttänyt muita lääkkeitä, myös lääkkeitä, joita lääkäri ei ole määrännyt.
Prostivas-valmisteen ja synnynnäistä sydänvikaa sairastavien vastasyntyneiden tavanomaisen lääkehoidon välillä ei ole raportoitu yhteisvaikutuksia. Tavanomaiseen lääkehoitoon kuuluvat antibiootit (kuten penisilliini tai gentamysiini), vasopressorit (kuten dopamiini), sydänglykosidit ja diureetit (kuten furosemidi).
Lapset
On todennäköistä, että Prostivas-valmisteen sisältämä alkoholi (etanoli) vaikuttaa lapsiin (ks. ”Prostivas sisältää alkoholia (etanolia)”).
Prostivas sisältää alkoholia (etanolia)
Prostivas sisältää 790 mg alkoholia (etanolia) per 1 ml:n injektiopullo, mikä vastaa 790 mg:aa/ml (79 % w/v). Alkoholimäärä 1 ml:n injektiopullossa vastaa alle 20 ml:aa olutta tai 8 ml:aa viiniä.
On todennäköistä, että tämän lääkevalmisteen sisältämä alkoholi vaikuttaa lapsiin. Vaikutuksia voivat olla uneliaisuus ja muutokset käytöksessä.
Tämä lääke annetaan hitaasti 24 tunnin aikana, joten etanolin vaikutukset voivat olla vähäisemmät.
Yhtäaikainen esim. propyleeniglykolia ja etanolia sisältävien lääkkeiden anto voi johtaa etanolin kertymiseen elimistöön ja aiheuttaa haittavaikutuksia etenkin pikkulapsille, joiden aineenvaihdunta on heikko tai kypsymätön.
Jos lapsellasi on epilepsia tai maksan toimintahäiriötä, keskustele lääkärin tai apteekkihenkilökunnan kanssa ennen tämän lääkkeen antamista lapsellesi.
Tämä lääkkeen sisältämä alkoholimäärä saattaa muuttaa muiden lääkkeiden vaikutusta. Keskustele lääkärin tai apteekkihenkilökunnan kanssa, jos lapsesi parhaillaan käyttää muita lääkkeitä.
3. Miten valmistetta käytetään
Prostivas infusoidaan infuusiopumpulla suureen laskimoon tai napavaltimokatetrin kautta.
Lääkäri määrittää annoksen lapselle yksilöllisesti. Jos sinulla on kysymyksiä tämän lääkkeen käytöstä, käänny lääkärin, apteekkihenkilökunnan tai sairaanhoitajan puoleen.
4. Mahdolliset haittavaikutukset
Kuten kaikki lääkkeet, myös Prostivas voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa.
Hyvin yleisiä haittavaikutuksia (esiintyy todennäköisesti useammalla kuin yhdellä henkilöllä kymmenestä):
Hengityskatkot, ohimenevä kuume
Yleisiä haittavaikutuksia (esiintyy todennäköisesti alle yhdellä potilaalla kymmenestä): Epileptiset kohtaukset, sydämen harva- tai tiheälyöntisyys, matala verenpaine, veren matala kaliumpitoisuus (kaliumvaje), ripuli, punoitus iholla (infuusiopaikassa)
Melko harvinaisia haittavaikutuksia (esiintyy todennäköisesti alle yhdellä potilaalla sadasta):
Mahalaukun tyhjenemiseste, mahan limakalvomuutokset, luun pinnasta ulospäin kasvavat luukohoumat, verisuonien heikentyminen
Pitkäkestoisessa Prostivas-hoidossa on havaittu pitkien luiden lisäkasvua. Lapsen valtimotiehyissä ja keuhkovaltimoissa voi ilmetä kudoksen heikkenemiseen viittaavia muutoksia. Näiden löydösten käytännön merkitystä ei kuitenkaan tiedetä.
Jos havaitset lapsellasi sellaisia haittavaikutuksia, joita ei ole tässä pakkausselosteessa mainittu, tai hänen kokemansa haittavaikutus on vakava, kerro niistä lääkärille tai apteekkihenkilökunnalle.
Haittavaikutuksista ilmoittaminen
Jos havaitset haittavaikutuksia, kerro niistä lääkärille, apteekkihenkilökunnalle tai sairaanhoitajalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Voit ilmoittaa haittavaikutuksista myös suoraan (ks. yhteystiedot alla). Ilmoittamalla haittavaikutuksista voit auttaa saamaan enemmän tietoa tämän lääkevalmisteen turvallisuudesta.
www‐sivusto: www.fimea.fi
Lääkealan turvallisuus‐ ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
00034 FIMEA
5. Valmisteen säilyttäminen
Ei lasten ulottuville eikä näkyville.
Infuusiokonsentraatti: Säilytä jääkaapissa (2–8 °C).
Älä käytä Prostivas-valmistetta pakkauksessa mainitun viimeisen käyttöpäivämäärän jälkeen. Viimeinen käyttöpäivämäärä tarkoittaa kuukauden viimeistä päivää.
Lääkkeitä ei tule heittää viemäriin eikä hävittää talousjätteiden mukana. Kysy käyttämättömien lääkkeiden hävittämisestä apteekista. Näin menetellen suojelet luontoa.
6. Pakkauksen sisältö ja muuta tietoa
Mitä Prostivas sisältää
- Vaikuttava aine on alprostadiili.
- Yksi ampulli sisältää 0,5 mg alprostadiilia (laimentaminen, ks. kohta 4.2).
- Muu aine on: etanoli (ks. kohta Mitä sinun on tiedettävä ennen valmisteen käyttöä ”Prostivas sisältää alkoholia (etanolia)”).
Lääkevalmisteen kuvaus ja pakkauskoot
Prostivas on pakattu ampulleihin. Valmiste on kirkas, väritön liuos.
Prostivas-valmisteesta on markkinoilla yhden ampullin pakkaus.
Myyntiluvan haltija ja valmistaja
Myyntiluvan haltija
Pfizer Oy
Tietokuja 4
00330 Helsinki
Valmistaja
Pfizer Manufacturing Belgium N.V./S.A., Puurs, Belgia
Tämä pakkausseloste on tarkastettu viimeksi: 12.4.2021.
Ohjeet terveydenhuollon ammattilaiselle
Ainoastaan lääketieteellisen koulutuksen saanut henkilökunta saa antaa alprostadiili-infuusiokonsentraattia tiloissa, joissa lapsipotilaille voidaan antaa tehohoitoa ja lasten teho-osasto on tarvittaessa käytettävissä.
Infuusiokonsentraatin laimentaminen
- Laimenna yksi Prostivas-ampulli (= 500 mikrog PGE1/1 ml) 100 ml:aan 0,9-prosenttista natriumkloridi-infuusionestettä tai 5-prosenttista steriiliä glukoosi-infuusionestettä.
- Koska alprostadiili on instabiili, se on säilytettävä jääkaapissa (2–8 °C).
- Valmista tuore alprostadiililaimennos 24 tunnin välein. Hävitä yli 24 tuntia vanhat laimennokset.
Infuusionopeus
0,6 ml/kg/h =
0,01 ml/kg/min =
0,05 mikrog/kg/min i.v.
Taulukossa esitetyt alprostadiilipitoisuudet (mikrog/ml) saavutetaan lisäämällä 100, 250 ja 500 mikrog alprostadiilia ilmoitettuihin laimenninmääriin:
| |
|
|
Alprostadiililisäys (mikrog)
|
|
Kokonaistilavuus
|
100 mikrog
(0,2 ml)*
|
250 mikrog
(0,5 ml)*
|
500 mikrog
(1,0 ml)*
|
|
250 ml
|
0,4
|
1,0
|
2,0
|
|
100 ml
|
1,0
|
2,5
|
5,0
|
|
50 ml
|
2,0
|
5,0
|
10,0
|
|
25 ml
|
4,0
|
10,0
|
20,0
|
*lisäys ml:na
Infuusionopeuden laskeminen:
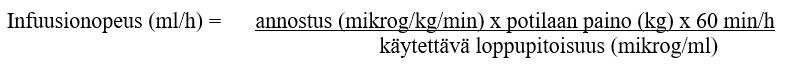
Esimerkki: 2,8-kiloiselle vastasyntyneelle annettava 0,1 mikrog/kg/min alprostadiilia, kun käytettävä loppupitoisuus on 5 mikrog/ml: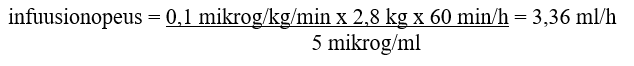
Annostus ja antotapa
Annostus
Aloita infuusio yleensä annoksella 0,05 - 0,1 mikrog alprostadiilia painokiloa kohti minuutissa. Kun hoitovaste on saavutettu, pienennä infuusioannos pienimpään mahdolliseen määrään, jolla toivotut vaikutukset säilyvät. Ylläpitoinfuusion sopiva nopeus on usein 0,01 mikrog/kg/min.
Jos aloitusannos 0,1 mikrog/kg/min ei riitä, annoksen voi varovasti suurentaa enimmäismäärään 0,4 mikrog/kg/min. Annoksen suurentaminen ei kuitenkaan yleensä paranna vastetta.
Antotapa
Prostivas-infuusiokonsentraatti on suositeltavinta antaa jatkuvana infuusiona suureen laskimoon. Se voidaan antaa myös valtimotiehyen aukkoon sijoitetun napavaltimokatetrin kautta. Valmiste lisää veren hapettumista (pO2) yhtä paljon antotavasta riippumatta.
Käytä infuusiossa infuusiopumppua, jonka infuusionopeutta voi säätää portaattomasti toivotun vasteen saavuttamiseksi.
Pediatriset potilaat
On todennäköistä, että Prostivas-valmisteen sisältämä etanoli vaikuttaa lapsiin.
Varoitukset ja käyttöön liittyvät varotoimet
Vastasyntyneellä voi ilmetä apneaa, joka alkaa yleensä ensimmäisen tunnin kuluessa infuusion aloittamisesta. Käytä valmistetta siis olosuhteissa, joissa mahdollinen hengitysvajaus voidaan hoitaa nopeasti. Mittaa valtimopaine ajoittain napavaltimokatetrilla, auskultoimalla tai Doppler-anturilla. Jos valtimopaine laskee huomattavasti, pienennä infuusionopeutta heti.
Yhteensopimattomuudet
Jos laimentamaton Prostivas-infuusiokonsentraatti joutuu suoraan kosketukseen muovisen infuusiopullon kanssa, pullon seinämistä saattaa liueta liuokseen muovinpehmittimiä. Liuos voi muuttua sameaksi ja muovin ulkonäkö muuttua. Hävitä tällöin liuos ja ota käyttöön uusi muovipullo. Reaktio riippuu pitoisuudesta. Samentumisen estämiseksi lisää Prostivas-infuusiokonsentraatti suoraan infuusionesteeseen välttäen suoraa kosketusta muovipullon kanssa.
Säilytys ja kestoaika
Infuusiokonsentraatti: Säilytä jääkaapissa (2–8 °C).
Laimennettu infuusiokonsentraatti: Prostivas-infuusiokonsentraatin laimennokset säilyvät laimentamisen jälkeen kemiallisesti ja fysikaalisesti 8 tuntia huoneenlämmössä tai 24 tuntia jääkaapissa.
Laimennettu liuos tulisi käyttää heti mikrobiologisista syistä. Jos liuosta ei käytetä heti, on vastuu säilytysajasta ja -olosuhteista ennen käyttöä käyttäjällä. Normaalisti säilytys saa kestää enintään 24 tuntia 2–8 °C:ssa, jos valmistetta ei ole liuotettu/laimennettu kontrolloiduissa ja validoiduissa aseptisissa olosuhteissa.
Hävitä käyttämättä jäänyt infuusioliuos.
Ei lasten ulottuville.
Älä käytä myyntipäällysmerkinnöissä olevan viimeisen käyttöpäivän jälkeen.