Bexsero injektioneste, suspensio, esitäytetyssä ruiskussa
B‑ryhmän meningokokkirokote (rDNA, nelikomponenttinen, adsorboitunut)
Yleisiä ohjeita
Lue tämä pakkausseloste huolellisesti ennen kuin sinä saat tai lapsesi saa tätä lääkettä, sillä se sisältää sinulle tai lapsellesi tärkeitä tietoja.
- Säilytä tämä pakkausseloste. Voit tarvita sitä myöhemmin.
- Jos sinulla on kysyttävää, käänny lääkärin tai sairaanhoitajan puoleen.
- Tämä rokote on määrätty vain sinulle tai lapsellesi.
- Jos havaitset haittavaikutuksia, kerro niistä lääkärille tai sairaanhoitajalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Ks. kohta Mahdolliset haittavaikutukset.
Tässä pakkausselosteessa kerrotaan
1. Mitä Bexsero on ja mihin sitä käytetään
2. Mitä sinun on tiedettävä, ennen kuin sinä saat tai lapsesi saa Bexseroa
3. Miten Bexseroa käytetään
4. Mahdolliset haittavaikutukset
5. Bexseron säilyttäminen
6. Pakkauksen sisältö ja muuta tietoa
1. Mitä valmiste on ja mihin sitä käytetään
Bexsero on rokote B‑ryhmän meningokokkia vastaan.
Bexsero sisältää neljää erilaista B‑ryhmän Neisseria meningitidis ‑bakteerin pintakomponenttia.
Bexseroa annetaan 2 kuukauden iästä lähtien suojaamaan Neisseria meningitidis ‑nimisen B‑ryhmän bakteerin aiheuttamalta sairaudelta. Nämä bakteerit voivat aiheuttaa vakavia, toisinaan hengenvaarallisia, infektioita, kuten aivokalvotulehduksen (aivoja ja selkäydintä peittävän kalvon tulehduksen) ja verenmyrkytyksen.
Rokote stimuloi rokotetun henkilön elimistön luontaista puolustusjärjestelmää. Tämä tuottaa suojan sairautta vastaan.
2. Mitä sinun on tiedettävä ennen valmisteen käyttöä
ÄLÄ käytä Bexseroa
- jos sinä olet tai lapsesi on allerginen vaikuttaville aineille tai tämän rokotteen jollekin muulle aineelle (lueteltu kohdassa Pakkauksen sisältö ja muuta tietoa).
Varoitukset ja varotoimet
Keskustele lääkärin tai sairaanhoitajan kanssa ennen kuin sinä saat tai lapsesi saa Bexseroa
- jos sinulla tai lapsellasi on vaikea infektio ja korkea kuume. Rokotusta on tällöin lykättävä. Lievä infektio, kuten vilustuminen, ei kuitenkaan edellytä rokotuksen lykkäämistä, mutta tarkista asia ensin lääkäriltä tai sairaanhoitajalta.
- jos sinulla tai lapsellasi on hemofilia tai muu syy, jonka vuoksi veresi ei hyydy normaalisti, kuten verenohennuslääkityksen (antikoagulanttien) käyttö. Keskustele ensin lääkärin tai sairaanhoitajan kanssa.
- jos sinä olet tai lapsesi on saanut immuunijärjestelmän komplementin aktivaatiota estävää hoitoa, kuten ekulitsumabi. Huolimatta siitä, että sinä olet tai lapsesi on saanut Bexsero-rokotuksen sinulla tai lapsellasi on suurentunut riski altistua Neisseria meningitidis ryhmän B bakteerin aiheuttamille taudeille.
- jos lapsesi on syntynyt ennenaikaisesti (28. raskausviikolla tai aiemmin) ja erityisesti, jos heillä oli hengitysvaikeuksia. Näillä lapsilla lyhytaikainen hengityksen pysähtyminen tai epäsäännöllinen hengitys voi olla kolmen ensimmäisen rokotuksen jälkeisen päivän aikana yleisempää. Nämä lapset voivat tarvita erityistä seurantaa.
- jos sinä olet tai lapsesi on allerginen kanamysiinille (antibiootille). Jos rokote sisältää kanamysiiniä, sitä on vain pieniä pitoisuuksia. Jos sinulla tai lapsellasi saattaa olla kanamysiiniallergia, keskustele ensin lääkärin tai sairaanhoitajan kanssa.
Neulanpisto voi aiheuttaa pyörtymisen, pyörryttävän olon tai muun stressiin liittyvän reaktion. Kerro lääkärille tai sairaanhoitajalle, jos sinulla on aiemmin ilmennyt tämäntyyppisiä reaktioita.
Bexseron käytöstä yli 50‑vuotiaille aikuisille ei ole tietoa. Bexseron käytöstä kroonisia sairauksia sairastaville potilaille tai potilaille, joiden vastustuskyky on heikentynyt on rajoitetusti tietoa. Jos sinulla tai lapsellasi on heikentynyt vastustuskyky (esimerkiksi immuunisuppressiivisten lääkkeiden käytön, HIV‑infektion tai elimistön luontaisen puolustusjärjestelmän perinnöllisen vajavuuden vuoksi), on mahdollista, että Bexseron teho on heikompi.
Bexsero, kuten mikään muukaan rokote, ei välttämättä anna täyttä suojaa kaikille rokotetuille.
Muut lääkevalmisteet ja Bexsero
Kerro lääkärille tai sairaanhoitajalle, jos parhaillaan käytät tai olet äskettäin käyttänyt tai saatat käyttää muita lääkkeitä tai lapsesi parhaillaan käyttää tai on äskettäin käyttänyt tai saattaa käyttää muita lääkkeitä tai jos olet tai lapsesi on äskettäin saanut jonkin muun rokotuksen.
Bexseroa voidaan antaa samanaikaisesti seuraavien rokotekomponenttien kanssa: kurkkumätä, jäykkäkouristus, hinkuyskä, Haemofilus influenzae tyyppi b (Hib), polio, B‑hepatiitti, pneumokokki, tuhkarokko, sikotauti, vihurirokko, vesirokko ja meningokokki A, C, W, Y. Kysy lisätietoja lääkäriltä tai sairaanhoitajalta.
Kun Bexsero annetaan samanaikaisesti muiden rokotteiden kanssa, se on annettava eri kohtaan.
Lääkäri tai sairaanhoitaja saattaa kehottaa sinua antamaan lapsellesi kuumetta alentavaa lääkettä Bexseron antamisen yhteydessä ja sen jälkeen. Näin voidaan vähentää joitakin Bexseron haittavaikutuksia.
Raskaus ja imetys
Jos olet raskaana tai imetät, epäilet olevasi raskaana tai jos suunnittelet lapsen hankkimista, kysy lääkäriltä neuvoa ennen kuin saat Bexseroa. Lääkäri saattaa silti suositella, että saat Bexsero‑rokotuksen, jos sinulla on meningokokki‑infektiolle altistumisen riski.
Ajaminen ja koneiden käyttö
Bexserolla ei ole haitallista vaikutusta ajokykyyn ja koneiden käyttökykyyn.
Jotkut kohdassa Mahdolliset haittavaikutukset Mahdolliset haittavaikutukset mainituista vaikutuksista saattavat kuitenkin vaikuttaa tilapäisesti ajokykyyn tai koneiden käyttökykyyn.
Bexsero sisältää natriumkloridia
Tämä lääkevalmiste sisältää alle 1 mmol natriumia (23 mg) per annos eli se on käytännössä natriumiton.
3. Miten valmistetta käytetään
Lääkäri tai sairaanhoitaja antaa Bexseron (0,5 ml) sinulle tai lapsellesi. Se pistetään lihakseen, vauvoilla yleensä reiteen ja lapsilla, nuorilla ja aikuisilla olkavarteen.
On tärkeää noudattaa lääkärin tai sairaanhoitajan ohjeita rokotussarjan loppuun ottamisesta.
Ensimmäisen annoksen antohetkellä 2-5 kuukauden ikäiset vauvat
Lapsesi saa kahden tai kolmen rokotuksen alkusarjan ja sen jälkeen vielä yhden rokotuksen (tehoste).
- Ensimmäinen rokotus annetaan aikaisintaan, kun vauva on 2 kuukauden ikäinen.
- Jos perusrokotussarjaan kuuluu kolme rokotusta, rokotusten antovälin on oltava vähintään 1 kuukausi.
- Jos perusrokotussarjaan kuuluu kaksi rokotusta, rokotusten antovälin on oltava vähintään 2 kuukautta.
- Tehoste annetaan 12–15 kuukauden iässä, kun perusrokotussarjan viimeisestä rokotuksesta on kulunut vähintään 6 kuukautta. Jos rokotuksen anto viivästyy, tehosterokotusta ei saa antaa 24 kuukauden iän jälkeen.
Ensimmäisen annoksen antohetkellä 6–11 kuukauden ikäiset vauvat
6–11 kuukauden ikäiset vauvat saavat kaksi rokotusta ja sen jälkeen vielä yhden (tehoste) rokotuksen.
- Rokotusten antovälin on oltava vähintään 2 kuukautta.
- Tehoste annetaan toisena elinvuotena, kun toisesta rokotuskerrasta on kulunut vähintään 2 kuukautta.
Ensimmäisen annoksen antohetkellä 12–23 kuukauden ikäiset lapset
12–23 kuukauden ikäiset lapset saavat kaksi rokotusta ja sen jälkeen vielä yhden (tehoste) rokotuksen.
- Rokotusten antovälin on oltava vähintään 2 kuukautta.
- Tehoste annetaan, kun toisesta rokotuskerrasta on kulunut 12–23 kuukautta.
Ensimmäisen annoksen antohetkellä 2–10 vuoden ikäiset lapset
2–10‑vuotiaat lapset saavat kaksi rokotusta.
- Rokotusten antovälin on oltava vähintään 1 kuukausi.
Lapsesi voi myös saada ylimääräisen rokotuksen (tehosterokotus).
Ensimmäisen annoksen antohetkellä vähintään 11‑vuotiaat nuoret ja aikuiset
Nuoret (vähintään 11‑vuotiaat) ja aikuiset saavat kaksi rokotusta.
- Rokotusten antovälin on oltava vähintään 1 kuukausi.
Voit myös saada ylimääräisen rokotuksen (tehosterokotus).
Yli 50‑vuotiaat aikuiset
Yli 50‑vuotiaista aikuisista ei ole tietoja. Kysy lääkäriltä neuvoa, onko Bexsero-rokotteesta sinulle hyötyä.
Jos sinulla on kysymyksiä Bexserosta, käänny lääkärin tai sairaanhoitajan puoleen.
4. Mahdolliset haittavaikutukset
Kuten kaikki rokotteet, tämäkin rokote voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa.
Kun sinulle tai lapsellesi annetaan Bexseroa, hyvin yleisiä (saattaa ilmetä useammalla kuin yhdellä rokotetulla kymmenestä) mahdollisesti ilmaantuvia haittavaikutuksia (joita on ilmoitettu kaikissa ikäryhmissä) ovat:
- kipu/aristus antopaikassa, ihon punoitus antopaikassa, ihon turvotus antopaikassa, ihon kovettuma antopaikassa.
Seuraavia haittavaikutuksia voi myös ilmaantua tämän rokotteen saamisen jälkeen.
Vauvat ja lapset (enintään 10‑vuotiaat)
Hyvin yleinen (näitä saattaa ilmetä useammin kuin yhdellä rokotetulla kymmenestä): kuume (38 °C kuume tai sitä korkeampi), ruokahaluttomuus, aristus antopaikassa (mukaan lukien vaikea‑asteinen antopaikan aristus, joka ilmenee itkuna kyseistä raajaa liikutettaessa), kivuliaat nivelet, ihottuma (12–23 kuukauden ikäiset lapset) (melko harvinainen tehosterokotuksen jälkeen), uneliaisuus, ärtyisyys, epätavallinen itku, oksentelu (melko harvinainen tehosterokotuksen jälkeen), ripuli, päänsärky.
Yleinen (näitä saattaa ilmetä enintään yhdellä rokotetulla kymmenestä): ihottuma (2–10‑vuotiaat vauvat ja lapset).
Melko harvinainen (näitä saattaa ilmetä enintään yhdellä rokotetulla sadasta): korkea kuume (40 °C kuume tai sitä korkeampi), kouristuskohtaukset (mukaan lukien kuumekouristukset), ihon kuivuminen, kalpeus (harvinaista tehosterokotuksen jälkeen).
Harvinainen (näitä saattaa ilmetä enintään yhdellä rokotetulla tuhannesta): Kawasakin tauti, johon voi liittyä oireina esim. yli viisi päivää kestävää kuumetta, johon liittyy ihottumaa vartalon alueella ja joskus ihon hilseilyä käsissä ja sormissa, turvonneita rauhasia kaulan alueella, punaiset silmät, huulet, kurkku ja kieli. Kutiava ihottuma, ihottuma.
Nuoret (vähintään 11‑vuotiaat) ja aikuiset
Hyvin yleinen (näitä saattaa ilmetä useammin kuin yhdellä rokotetulla kymmenestä): kipu antopaikassa, mikä aiheuttaa kyvyttömyyden suoriutua normaaleista päivittäisistä toimista, lihas‑ ja nivelkivut, pahoinvointi, yleinen sairaudentunne, päänsärky.
Valmisteen markkinoilletulon jälkeen on ilmoitettu seuraavia haittavaikutuksia:
Suurentuneet imusolmukkeet.
Allergiset reaktiot, mm. voimakas turvotus huulissa, suussa, kurkussa (mikä voi aiheuttaa nielemisvaikeuksia), hengitysvaikeudet ja niihin liittyvä hengityksen vinkuminen tai yskiminen, ihottuma, tajunnan menetys ja hyvin matala verenpaine.
Kollapsi (lihasten äkillinen veltostuminen), poissaolokohtaukset tai huomiokyvyn heikkeneminen, kalpeus tai sinertävä ihon väri nuorilla lapsilla.
Pyörryttävä olo tai pyörtyminen.
Ihottuma (aikuisilla ja nuorilla 11-vuotiaasta lähtien).
Kuume (aikuisilla ja nuorilla 11-vuotiaasta lähtien).
Injektiokohdan reaktiot kuten rokotetun raajan laaja turpoaminen, rakkulat antopaikassa tai sen ympärillä ja injektiokohdassa oleva kova patti, joka voi pysyä yli kuukauden ajan).
Niskan jäykkyyttä tai epämiellyttävää herkkyyttä valolle (valonarkuus), jotka ovat merkkejä aivokalvoärsytyksestä, on satunnaisesti raportoitu pian rokotuksen jälkeen; nämä oireet ovat olleet lieviä ja ohimeneviä.
Haittavaikutuksista ilmoittaminen
Jos havaitset haittavaikutuksia, kerro niistä lääkärille, apteekkihenkilökunnalle tai sairaanhoitajalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Voit ilmoittaa haittavaikutuksista myös suoraan kansallisen ilmoitusjärjestelmän kautta. Ilmoittamalla haittavaikutuksista voit auttaa saamaan enemmän tietoa tämän lääkevalmisteen turvallisuudesta.
www-sivusto: www.fimea.fi
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
00034 FIMEA
5. Valmisteen säilyttäminen
Ei lasten ulottuville eikä näkyville.
Älä käytä tätä rokotetta pakkauksessa ja esitäytetyn ruiskun etiketissä mainitun viimeisen käyttöpäivämäärän (Käyt. viim.) jälkeen. Viimeinen käyttöpäivämäärä tarkoittaa kuukauden viimeistä päivää.
Säilytä jääkaapissa (2 °C–8 °C). Ei saa jäätyä.
Säilytä alkuperäispakkauksessa. Herkkä valolle.
Lääkkeitä ei pidä heittää viemäriin eikä hävittää talousjätteiden mukana. Kysy käyttämättömien lääkkeiden hävittämisestä lääkäriltä tai sairaanhoitajalta. Näin menetellen suojelet luontoa.
6. Pakkauksen sisältö ja muuta tietoa
Mitä Bexsero sisältää
Yksi annos (0,5 ml) sisältää:
Vaikuttavat aineet:
|
Rekombinanttia B‑ryhmän Neisseria meningitidis ‑bakteerin NHBA‑fuusioproteiinia1, 2, 3
|
50 mikrogrammaa
|
|
Rekombinanttia B‑ryhmän Neisseria meningitidis ‑bakteerin NadA‑proteiinia1, 2, 3
|
50 mikrogrammaa
|
|
Rekombinanttia B‑ryhmän Neisseria meningitidis ‑bakteerin fHbp‑fuusioproteiinia1, 2, 3
|
50 mikrogrammaa
|
|
B‑ryhmän Neisseria meningitidis ‑kannan NZ98/254 ulkokalvovesikkeleitä (OMV) PorA P1.4:ää sisältävänä kokonaisproteiinimääränä mitattuna2
|
25 mikrogrammaa
|
1 tuotettu E. coli ‑soluissa yhdistelmä‑DNA‑tekniikalla
2 adsorboitu alumiinihydroksidiin (0,5 mg Al³+).
3 NHBA (Neisserial Heparin Binding Antigen), NadA (Neisseria adhesin A), fHbp (factor H binding protein)
Muut aineet:
natriumkloridi, histidiini, sakkaroosi ja injektionesteisiin käytettävä vesi (katso kohdasta Mitä sinun on tiedettävä ennen valmisteen käyttöä lisätietoa natriumista).
Lääkevalmisteen kuvaus ja pakkauskoot
Bexsero on valkoinen, opalisoiva suspensio.
Bexsero on saatavana yhden annoksen esitäytetyssä ruiskussa erillisillä neuloilla tai ilman, pakkauskoot 1 ja 10.
Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
Myyntiluvan haltija:
GSK Vaccines S.r.l.
Via Fiorentina 1
53100 Siena
Italia
Valmistaja:
GSK Vaccines S.r.l.
Bellaria‑Rosia
53018 Sovicille (Siena)
Italia
Lisätietoja tästä lääkevalmisteesta antaa myyntiluvan haltijan paikallinen edustaja:
Suomi/Finland
GlaxoSmithKline Oy
Puh/Tel: + 358 10 30 30 30
Tämä pakkausseloste on tarkistettu viimeksi 26.4.2023
Lisätietoa tästä lääkevalmisteesta on saatavilla Euroopan lääkeviraston verkkosivulla http://www.ema.europa.eu.
Ohjeet terveydenhuollon ammattilaiselle
Suspension sisältävään esitäytettyyn ruiskuun on havaittu muodostuneen säilytyksen aikana hienojakoista luonnonvalkoista sakkaa.
Ravista esitäytettyä ruiskua hyvin ennen käyttöä, jotta muodostuu homogeeninen suspensio.
Rokote on tarkastettava silmämääräisesti hiukkasten ja värimuutosten havaitsemiseksi ennen antoa.
Jos vierashiukkasia ja/tai fysikaalisia muutoksia havaitaan, rokotetta ei saa antaa. Jos pakkauksessa toimitetaan kaksi eripituista neulaa, niistä on valittava asianmukainen neula, jolla varmistetaan rokotteen anto lihakseen.
Ei saa jäätyä.
Bexseroa ei saa sekoittaa samaan ruiskuun muiden rokotteiden kanssa.
Jos muiden rokotteiden antaminen samanaikaisesti on tarpeen, rokotteet on annettava eri kohtiin.
On varmistuttava siitä, että rokote annetaan vain lihakseen.
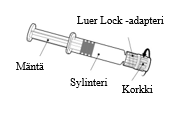
Esitäytetyn ruiskun käyttöohje
|
|
Pidä kiinni ruiskun sylinteristä, ei männästä.
Poista ruiskun korkki kiertämällä
vastapäivään.
|
|
|
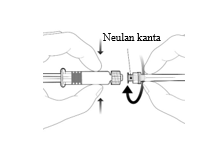
Neula kiinnitetään ruiskuun yhdistämällä neulan kanta Luer Lock -adapteriin ja kiertämällä neulaa neljänneskierros myötäpäivään, kunnes neula tuntuu kiinnittyvän ruiskuun.
Korkki
Älä vedä ruiskun mäntää ulos sylinteristä.
Jos mäntä irtoaa sylinteristä, älä anna
rokotetta.
|
Hävitys
Käyttämätön lääkevalmiste tai jäte on hävitettävä paikallisten vaatimusten mukaisesti.