Trazimera 150 mg kuiva-aine välikonsentraatiksi infuusionestettä varten, liuos
Trazimera 420 mg kuiva-aine välikonsentraatiksi infuusionestettä varten, liuos
trastutsumabi
Yleisiä ohjeita
Lue tämä pakkausseloste huolellisesti, ennen kuin aloitat tämän lääkkeen käyttämisen, sillä se sisältää sinulle tärkeitä tietoja.
- Säilytä tämä pakkausseloste. Voit tarvita sitä myöhemmin.
- Jos sinulla on kysyttävää, käänny lääkärin tai apteekkihenkilökunnan puoleen.
- Jos havaitset haittavaikutuksia, kerro niistä lääkärille, apteekkihenkilökunnalle tai sairaanhoitajalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Ks. kohta Mahdolliset haittavaikutukset.
Tässä pakkausselosteessa kerrotaan
- Mitä Trazimera on ja mihin sitä käytetään
- Mitä sinun on tiedettävä, ennen kuin sinulle annetaan Trazimera-valmistetta
- Miten Trazimera annetaan
- Mahdolliset haittavaikutukset
- Trazimera-valmisteen säilyttäminen
- Pakkauksen sisältö ja muuta tietoa
1. Mitä valmiste on ja mihin sitä käytetään
Trazimera-valmisteen vaikuttavana aineena on trastutsumabi, joka on monoklonaalinen vasta-aine. Monoklonaaliset vasta-aineet sitoutuvat tiettyihin proteiineihin tai antigeeneihin. Trastutsumabi on tarkoitettu sitoutumaan valikoivasti antigeeniin, jota kutsutaan ihmisen epidermaalisen kasvutekijän reseptori 2:ksi (HER2). HER2:ta esiintyy suurina määrinä tiettyjen syöpäsolujen pinnalla, joissa se stimuloi näiden kasvua. Trastutsumabin sitoutuminen HER2:een pysäyttää kyseisten syöpäsolujen kasvun, mistä on seurauksena syöpäsolun kuolema.
Lääkäri saattaa määrätä Trazimera-valmistetta hoidoksi rintasyöpään tai mahasyöpään, jos
- sinulla on varhaisen vaiheen rintasyöpä, joka tuottaa suuria määriä HER2-nimistä proteiinia.
- sinulla on etäpesäkkeinen rintasyöpä (rintasyöpä on levinnyt alkuperäisestä kasvaimesta muualle elimistöön) ja syöpäkasvaimet tuottavat suuria määriä HER2:ta. Trazimera-valmistetta voidaan määrätä ensimmäisenä hoitona yhdessä solunsalpaajiin kuuluvien paklitakselin tai dosetakselin kanssa etäpesäkkeisessä rintasyövässä. Valmistetta käytetään myös yksinään tilanteissa, joissa muu hoito ei ole ollut tehokasta. Sitä käytetään myös yhdessä niin sanottujen aromataasinestäjien kanssa potilaille, joilla on HER2-positiivinen ja hormonireseptoripositiivinen levinnyt rintasyöpä (syöpä, joka on herkkä naisen sukupuolihormoneille).
- sinulla on etäpesäkkeinen mahasyöpä, joka tuottaa suuria määriä HER2:ta. Valmistetta käytetään yhdessä muihin syöpälääkkeisiin kuuluvien kapesitabiinin tai 5-fluorourasiilin ja sisplatiinin kanssa.
2. Mitä sinun on tiedettävä ennen valmisteen käyttöä
Älä käytä Trazimera-valmistetta
- jos olet allerginen trastutsumabille, hiiren proteiineille tai tämän lääkkeen jollekin muulle aineelle (lueteltu kohdassa Pakkauksen sisältö ja muuta tietoa).
- jos sinulla on vaikeita syövästäsi johtuvia hengitysvaikeuksia levossa tai jos tarvitset lisähappea.
Varoitukset ja varotoimet
Lääkäri tulee seuraamaan hoitoasi tarkoin.
Sydämen toiminnan seuranta
Trazimera-hoito yksinään tai yhdistettynä taksaaniin saattaa vaikuttaa sydämeen, erityisesti jos olet käyttänyt aiemmin antrasykliinejä (taksaanit ja antrasykliinit ovat muita syöpälääkkeitä). Vaikutukset saattavat olla kohtalaisia tai vaikeita ja saattavat johtaa kuolemaan. Tämän vuoksi sydämen toiminta tutkitaan ennen Trazimera-hoidon aloittamista ja sitä seurataan hoidon aikana (joka kolmas kuukausi) ja seurantaa jatketaan hoidon lopettamisen jälkeen (kahdesta viiteen vuoteen). Jos sinulle kehittyy sydämen vajaatoiminnan oireita (eli sydän ei pumppaa riittävästi verta), sydämesi toiminta saatetaan tutkia tiheämmin (kuudesta kahdeksaan viikon välein) ja saatat saada hoitoa sydämen vajaatoimintaan tai Trazimera-hoito saattaa olla tarpeen lopettaa.
Keskustele lääkärin, apteekkihenkilökunnan tai sairaanhoitajan kanssa ennen kuin sinulle annetaan Trazimera-valmistetta,
- jos sinulla on ollut sydämen vajaatoimintaa, sepelvaltimotauti, sydämen läppävika (sydämen sivuäänet), korkea verenpaine tai jos olet ottanut verenpainelääkkeitä tai parhaillaan otat jotakin verenpainelääkettä.
- jos olet joskus aiemmin saanut tai parhaillaan käytät doksorubisiinia tai epirubisiinia (syöpälääkkeitä). Nämä lääkeaineet (tai muut antrasykliinit) voivat vahingoittaa sydänlihasta ja lisätä sydänongelmien riskiä Trazimera-hoidon aikana.
- jos sinulla on hengästyneisyyttä, etenkin jos parhaillaan käytät jotakin taksaania. Trazimera saattaa aiheuttaa hengitysvaikeuksia, erityisesti ensimmäisellä antokerralla. Oireet saattavat olla vakavampia, jos sinulla esiintyy valmiiksi hengästyneisyyttä. Hyvin harvoissa tapauksissa potilaat, joilla on ollut vaikeita hengitysvaikeuksia jo ennen hoidon aloittamista, ovat kuolleet annettaessa trastutsumabia.
- jos sinulle on aiemmin annettu muita syöpähoitoja.
Jos sinulle annetaan Trazimera-valmistetta yhdessä minkä tahansa syöpälääkkeen, kuten paklitakselin, dosetakselin, aromataasinestäjän, kapesitabiinin, 5-fluorourasiilin tai sisplatiinin, kanssa, sinun tulee lukea myös näiden valmisteiden pakkausselosteet.
Lapset ja nuoret
Trazimera-valmistetta ei suositella alle 18-vuotiaille.
Muut lääkevalmisteet ja Trazimera
Kerro lääkärille, apteekkihenkilökunnalle tai sairaanhoitajalle, jos parhaillaan otat tai olet äskettäin ottanut tai saatat ottaa muita lääkkeitä.
Trazimera-valmisteen poistuminen elimistöstä saattaa kestää jopa 7 kuukautta. Tämän vuoksi sinun pitää kertoa lääkärille, apteekkihenkilökunnalle tai sairaanhoitajalle saaneesi Trazimera-valmistetta, jos aloitat minkä tahansa uuden lääkkeen käytön 7 kuukauden sisällä hoidon lopettamisesta.
Raskaus
- Jos olet raskaana, epäilet olevasi raskaana tai jos suunnittelet lapsen hankkimista, kysy lääkäriltä, apteekista tai sairaanhoitajalta neuvoa ennen tämän lääkkeen käyttöä.
- Sinun on käytettävä tehokasta raskaudenehkäisyä Trazimera-hoidon aikana ja ainakin 7 kuukauden ajan hoidon päätyttyä.
- Lääkäri neuvoo sinua raskaudenaikaisen Trazimera-hoidon mahdollisista hyödyistä ja haitoista. Harvinaisissa tapauksissa lapsiveden (ympäröi kehittyvää lasta kohdussa) niukkuutta on havaittu Trazimera-valmistetta saavilla raskaana olevilla naisilla. Lapsiveden vähyys saattaa olla haitallinen sikiölle, ja se on yhdistetty heikentyneeseen keuhkojen kehittymiseen ja tästä johtuviin sikiökuolemiin.
Imetys
Älä imetä lasta Trazimera-hoidon aikana äläkä 7 kuukauteen viimeisestä Trazimera-annoksesta laskettuna, koska lapsi saattaa saada Trazimera-valmistetta rintamaidon välityksellä.
Kysy lääkäriltä tai apteekista neuvoa ennen minkään lääkkeen käyttöä.
Ajaminen ja koneiden käyttö
Trazimera saattaa vaikuttaa kykyysi ajaa autoa tai käyttää koneita. Jos sinulla ilmenee Trazimera-hoidon aikana oireita, kuten huimausta, uneliaisuutta, vilunväristyksiä tai kuumetta, sinun ei pidä ajaa autoa eikä käyttää koneita, ennen kuin oireet ovat lakanneet.
3. Miten valmistetta käytetään
Ennen hoidon aloittamista lääkäri määrittää HER2:n määrän kasvaimestasi. Trazimera-valmisteella hoidetaan vain potilaita, joilla HER2-pitoisuus on suuri. Trazimera-valmisteen saa antaa vain lääkäri tai sairaanhoitaja. Lääkärisi tulee määräämään sinulle sopivan annoksen ja hoito-ohjelman. Trazimera-annos määräytyy painosi mukaan.
Laskimoon annettavaa Trazimera-valmistetta ei ole tarkoitettu annettavaksi ihon alle, joten sitä saa antaa vain infuusiona laskimoon.
Trazimera-valmisteen laskimonsisäinen lääkemuoto annetaan laskimonsisäisenä infuusiona (tiputuksena) suoraan laskimoon. Ensimmäinen hoitoannos annetaan 90 minuutin infuusiona. Terveydenhuollon ammattilainen seuraa vointiasi infuusion ajan mahdollisten haittavaikutusten havaitsemiseksi. Jos siedät ensimmäisen annoksen hyvin, seuraavat annokset voidaan antaa 30 minuutissa (ks. kohta Mitä sinun on tiedettävä ennen valmisteen käyttöä, Varoitukset ja varotoimet). Saamiesi infuusioiden lukumäärä riippuu siitä, kuinka hoito vaikuttaa sinuun (hoitovasteestasi). Lääkärisi keskustelee kanssasi tästä.
Lääkitysvirheiden välttämiseksi on tärkeää varmistaa injektiopullon etiketistä, että valmistettava ja annettava lääkevalmiste on Trazimera (trastutsumabi) eikä toinen trastutsumabia sisältävä valmiste (esim. trastutsumabiemtansiini tai trastutsumabi-derukstekaani).
Varhaisen vaiheen rintasyövässä, metastasoituneessa rintasyövässä ja metastasoituneessa mahasyövässä Trazimera-valmistetta annetaan 3 viikon välein. Metastasoituneessa rintasyövässä Trazimera-valmistetta saatetaan antaa myös kerran viikossa.
Jos lopetat Trazimera-valmisteen käytön
Älä lopeta tämän lääkkeen käyttöä keskustelematta ensin lääkärin kanssa. Kaikki annokset on otettava oikeana ajankohtana viikon tai kolmen viikon välein (sinulle määrätyn annostuksen mukaisesti). Näin lääke vaikuttaa parhaalla mahdollisella tavalla.
Trazimera-valmisteen poistuminen elimistöstä saattaa kestää 7 kuukautta. Lääkäri saattaa siksi jatkaa sydämesi toiminnan seurantaa vielä hoidon päättymisen jälkeen.
Jos sinulla on kysymyksiä tämän lääkkeen käytöstä, käänny lääkärin, apteekkihenkilökunnan tai sairaanhoitajan puoleen.
4. Mahdolliset haittavaikutukset
Kuten kaikki lääkkeet, tämäkin lääke (Trazimera) voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa. Jotkin niistä voivat olla vakavia ja vaatia sairaalahoitoa.
Trazimera-infuusion aikana voi esiintyä vilunväristyksiä, kuumetta tai muita flunssan tapaisia oireita. Nämä haittavaikutukset ovat hyvin yleisiä (voi esiintyä yli yhdellä henkilöllä kymmenestä). Muita infuusioon liittyviä oireita ovat pahoinvointi, oksentelu, kipu, lisääntynyt lihasjänteys ja vapina, päänsärky, huimaus, hengitysvaikeudet, korkea tai matala verenpaine, sydämen rytmihäiriöt (tykytykset, sydämen läpätys tai epäsäännöllinen sydämen syke), kasvojen ja huulten turvotus, ihottuma ja väsymyksentunne. Osa näistä oireista voi olla vakavia, ja ne ovat joskus johtaneet potilaan kuolemaan (ks. kohta Mitä sinun on tiedettävä ennen valmisteen käyttöä, Varoitukset ja varotoimet).
Näitä oireita ilmenee pääasiallisesti ensimmäisen laskimoon annetun infuusion (tiputus laskimoon) yhteydessä ja muutaman tunnin aikana infuusion aloittamisesta. Oireet ovat yleensä ohimeneviä. Terveydenhoidon ammattilainen seuraa vointiasi infuusion ajan sekä vähintään 6 tunnin ajan ensimmäisen infuusion aloittamisesta ja 2 tunnin ajan seuraavien infuusioiden aloittamisesta. Jos sinulle kehittyy reaktio, infuusionopeutta hidastetaan tai infuusio lopetetaan ja sinulle saatetaan antaa hoitoa haittavaikutuksiin. Infuusiota voidaan jatkaa oireiden lievennettyä.
Satunnaisesti oireet voivat alkaa yli kuuden tunnin kuluttua infuusion aloittamisen jälkeen. Jos näin käy, ota välittömästi yhteyttä lääkäriin. Joskus oireet saattavat lievittyä mutta voivat pahentua myöhemmin.
Vakavat haittavaikutukset
Muita haittavaikutuksia voi esiintyä milloin tahansa Trazimera-hoidon aikana eikä vain infuusion antoon liittyvinä. Jos havaitset jonkin seuraavista haittavaikutuksista, kerro siitä heti lääkärille tai sairaanhoitajalle:
- Sydänongelmia saattaa toisinaan esiintyä hoidon aikana tai satunnaisesti hoidon jälkeen, ja ne voivat olla vakavia. Näihin kuuluvat sydänlihaksen heikkeneminen, joka saattaa johtaa sydämen vajaatoimintaan, sydäntä ympäröivän pussin tulehdukseen ja sydämen rytmihäiriöihin. Nämä saattavat ilmetä mm. seuraavina oireina: hengitysvaikeudet (myös yöllisiä), yskä, nesteen kertyminen jalkoihin tai käsivarsiin (turvotus), sydämentykytys (sydämen läpätys tai epäsäännöllinen sydämen syke) (ks. kohta Mitä sinun on tiedettävä ennen valmisteen käyttöä, Sydämen toiminnan seuranta).
Lääkäri tarkkailee sydäntäsi säännöllisesti hoidon aikana ja hoidon jälkeen, mutta sinun tulee kertoa hänelle välittömästi, jos huomaat jonkin edellä mainituista oireista.
- Tuumorilyysioireyhtymä (ryhmä syöpähoidon jälkeen ilmeneviä aineenvaihduntaan liittyviä lisätauteja, joille tyypillisiä ovat suuret kalium- ja fosfaattipitoisuudet veressä sekä pieni kalsiumpitoisuus veressä). Oireita voivat olla munuaisvaivat (heikotus, hengenahdistus, uupumus ja sekavuus), sydänvaivat (sydämen läpätys tai tavanomaista nopeampi tai hitaampi sydämen syke), kouristukset, oksentelu tai ripuli ja kihelmöinti suussa, käsissä tai jalkaterissä.
Jos sinulla ilmenee jokin yllä mainituista oireista Trazimera-hoidon päättymisen jälkeen, mene lääkäriin ja kerro hänelle Trazimera-hoidostasi.
Hyvin yleiset (voi esiintyä yli 1 henkilöllä kymmenestä):
- infektiot
- ripuli
- ummetus
- närästys (dyspepsia)
- uupumus
- ihottumat
- rintakipu
- vatsakipu
- nivelkipu
- punasolujen ja valkosolujen (auttavat elimistöä puolustautumaan tulehdusta vastaan) määrän vähentyminen, johon voi joskus liittyä kuumetta
- lihaskipu
- sidekalvotulehdus
- liiallinen kyynelnesteen eritys
- nenäverenvuodot
- vuotava nenä
- hiustenlähtö
- vapina
- kuumat aallot
- huimaus
- kynsimuutokset
- painonlasku
- ruokahaluttomuus
- unettomuus (insomnia)
- makuhäiriö
- alhainen verihiutalemäärä
- mustelmat
- sormien ja varpaiden puutuminen tai pistely, mikä toisinaan saattaa ulottua koko raajaan
- suun ja/tai nielun punoitus, turpoaminen tai haavaumat
- käsien ja/tai jalkaterien kipu, turpoaminen, punoitus tai pistely
- hengästyneisyys
- päänsärky
- yskä
- oksentelu
- pahoinvointi.
Yleiset (voi esiintyä enintään 1 henkilöllä kymmenestä):
- allergiset reaktiot
- kurkkuinfektiot
- virtsarakon ja ihon tulehdukset
- rintatulehdus
- maksatulehdus
- munuaisten toimintahäiriö
- lisääntynyt lihasjänteys (hypertonia)
- käsivarsien ja/tai jalkojen kipu
- kutiseva ihottuma
- uneliaisuus (somnolenssi)
- peräpukamat
- kutina
- suun ja ihon kuivuminen
- silmien kuivuus
- hikoilu
- heikkouden tunne ja huonovointisuus
- ahdistuneisuus
- masentuneisuus
- astma
- keuhkoinfektio
- keuhkojen toimintahäiriöt
- selkäkipu
- niskakipu
- luukipu
- akne
- jalkakrampit
Melko harvinaiset (voi esiintyä enintään 1 henkilöllä sadasta):
- kuurous
- näppyläinen ihottuma
- hengityksen vinkuminen
- keuhkojen tulehdus tai arpeutuminen.
Harvinaiset (voi esiintyä enintään 1 henkilöllä tuhannesta):
- keltaisuus
- anafylaktiset reaktiot.
Tuntematon (saatavilla oleva tieto ei riitä yleisyyden arviointiin):
- poikkeavuudet veren hyytymisessä tai heikentynyt veren hyytyminen
- korkea kaliumpitoisuus
- silmäntakainen turvotus tai verenvuoto
- sokki
- sydämen rytmihäiriöt
- hengitysvaikeudet
- hengitysvajaus
- akuutti nesteenkertyminen keuhkoihin
- akuutti ilmateiden ahtauma
- normaalia alhaisempi happipitoisuus veressä
- hengitysvaikeudet makuulla
- maksan vaurio
- kasvojen, huulien ja nielun turvotus
- munuaisten vajaatoiminta
- normaalia vähäisempi lapsiveden (ympäröi kehittyvää lasta kohdussa) määrä
- sikiön keuhkojen vajaakehitys kohdussa
- poikkeavuudet kohdussa tapahtuvassa sikiön munuaisten kehittymisessä.
Osa kokemistasi haittavaikutuksista saattaa johtua perussairaudestasi eli syövästä. Jos saat Trazimera-valmistetta yhdessä solunsalpaajahoidon kanssa, osa oireista saattaa liittyä myös solunsalpaajahoitoon.
Jos havaitset haittavaikutuksia, kerro niistä lääkärillesi tai apteekkihenkilökunnalle tai sairaanhoitajalle.
Haittavaikutuksista ilmoittaminen
Jos havaitset haittavaikutuksia, kerro niistä lääkärille, apteekkihenkilökunnalle tai sairaanhoitajalle.
Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Voit ilmoittaa haittavaikutuksista myös suoraan (ks. yhteystiedot alla). Ilmoittamalla haittavaikutuksista voit auttaa saamaan enemmän tietoa tämän lääkevalmisteen turvallisuudesta.
www‐sivusto: www.fimea.fi
Lääkealan turvallisuus‐ ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
00034 FIMEA
5. Valmisteen säilyttäminen
Ei lasten ulottuville eikä näkyville.
Älä käytä tätä lääkettä ulkokotelossa ja injektiopullon etiketissä mainitun viimeisen käyttöpäivämäärän (EXP) jälkeen. Viimeinen käyttöpäivämäärä tarkoittaa kuukauden viimeistä päivää.
Säilytä jääkaapissa (2 °C–8 °C).
Säilytä alkuperäispakkauksessa. Herkkä valolle.
Avaamattomia Trazimera-injektiopulloja voi säilyttää alle 30 °C:ssa yhden korkeintaan 3 kuukauden ajanjakson ajan. Jääkaappisäilytyksestä poiston jälkeen Trazimera-valmistetta ei saa laittaa takaisin jääkaappisäilytykseen. Hävitä Trazimera tämän 3 kuukauden jakson päätyttyä tai injektiopulloon merkittyyn viimeiseen käyttöpäivämäärään mennessä sen mukaan, kumpi näistä on ensin. Merkitse ”Hävitä viimeistään” ‑päivämäärä kotelossa sille varattuun kohtaan.
Infuusioliuokset on käytettävä heti laimentamisen jälkeen. Älä käytä Trazimera-valmistetta, jos huomaat näkyviä muutoksia lääkevalmisteen ulkonäössä (hiukkasia tai värimuutoksia) ennen annostelua.
Lääkkeitä ei pidä heittää viemäriin eikä hävittää talousjätteiden mukana. Kysy käyttämättömien lääkkeiden hävittämisestä apteekista. Näin menetellen suojelet luontoa.
6. Pakkauksen sisältö ja muuta tietoa
Mitä Trazimera sisältää
- Vaikuttava aine on trastutsumabi. Yksi injektiopullo sisältää joko
- 150 mg trastutsumabia, joka liuotetaan 7,2 ml:aan steriiliä injektionesteisiin käytettävää vettä tai
- 420 mg trastutsumabia, joka liuotetaan 20 ml:aan steriiliä injektionesteisiin käytettävää vettä.
Saatu liuos sisältää trastutsumabia noin 21 mg/ml.
- Muut aineet ovat L-histidiinihydrokloridimonohydraatti, L-histidiini, sakkaroosi, polysorbaatti 20 (E432).
Lääkevalmisteen kuvaus ja pakkauskoko
Trazimera kuiva-aine välikonsentraatiksi infuusionestettä varten, liuos, on pakattu kumitulpalliseen lasiseen injektiopulloon, joka sisältää joko 150 mg tai 420 mg trastutsumabia. Kuiva-aine on valkoisen kakun muodossa. Yksi kotelo sisältää yhden kuiva-ainetta sisältävän injektiopullon.
Myyntiluvan haltija
Pfizer Europe MA EEIG
Boulevard de la Plaine 17
1050 Bruxelles
Belgia
Valmistaja
Pfizer Manufacturing Belgium NV
Rijksweg 12
2870 Puurs-Sint-Amands
Belgia
Lisätietoja tästä lääkevalmisteesta antaa myyntiluvan haltijan paikallinen edustaja:
Suomi/Finland
Pfizer Oy
Puh/Tel: +358 (0)9 430 040
Tämä pakkausseloste on tarkistettu viimeksi 12/2024.
Muut tiedonlähteet
Lisätietoa tästä lääkevalmisteesta on saatavilla Euroopan lääkeviraston verkkosivulla https://www.ema.europa.eu.
Tämä pakkausseloste on saatavissa kaikilla EU-kielillä Euroopan lääkeviraston verkkosivustolla.
Ohjeet terveydenhuollon ammattilaiselle
Laskimoon annettava Trazimera on steriilissä, pyrogeenittomassa, kertakäyttöisessä injektiopullossa, joka ei sisällä säilytysainetta.
Lääkitysvirheiden välttämiseksi on tärkeää varmistaa injektiopullon etiketistä, että valmistettava ja annettava lääkevalmiste on Trazimera (trastutsumabi) eikä toinen trastutsumabia sisältävä valmiste (esim. trastutsumabiemtansiini tai trastutsumabi-derukstekaani).
Tämä lääke on aina säilytettävä suljetussa alkuperäispakkauksessaan jääkaapissa, 2 °C–8 °C:n lämpötilassa.
Avaamattomia Trazimera-injektiopulloja voi säilyttää alle 30 °C:ssa yhden korkeintaan 3 kuukauden ajanjakson ajan. Jääkaappisäilytyksestä poiston jälkeen Trazimera-valmistetta ei saa laittaa takaisin jääkaappisäilytykseen. Hävitä Trazimera tämän 3 kuukauden jakson päätyttyä tai injektiopulloon merkittyyn viimeiseen käyttöpäivämäärään mennessä sen mukaan, kumpi näistä on ensin. Merkitse ”Hävitä viimeistään” ‑päivämäärä kotelossa sille varattuun kohtaan.
9 mg/ml (0,9 %) natriumkloridiliuoksella aseptisesti laimennetut Trazimera-liuokset laskimoinfuusioon säilyvät fysikaalisesti ja kemiallisesti stabiileina enintään 30 vuorokautta 2 °C–8 °C:ssa ja 24 tuntia alle 30 °C:ssa.
Mikrobiologiselta kannalta katsottuna liuotettu infuusiokuiva-aine ja valmis Trazimera-infuusioliuos tulisi käyttää heti. Mikäli liuotettua ja/tai laimennettua valmistetta ei käytetä heti, säilytysajat ja -olosuhteet ennen käyttöä ovat käyttäjän vastuulla, eivätkä saa tavallisesti ylittää 24 tuntia 2 °C–8 °C:ssa, paitsi jos valmiste on liuotettu ja laimennettu kontrolloiduissa ja validoiduissa aseptisissa olosuhteissa.
Liuottamisessa ja laimentamisessa on käytettävä soveltuvaa aseptista tekniikkaa. Valmistettavien liuosten steriiliys on varmistettava huolellisesti. Tämä lääkevalmiste ei sisällä antimikrobisia säilytysaineita eikä bakteriostaattisia aineita, joten sitä on käsiteltävä aseptisesti.
Aseptinen käyttökuntoon saattaminen, käsittely ja säilytys
Infuusion käyttökuntoon saattamisessa on noudatettava aseptista toimintatapaa.
- Käyttökuntoon saattaminen on tehtävä aseptisissa olosuhteissa. Koulutettu henkilökunta saattaa infuusion käyttökuntoon hyvien toimintatapojen mukaisesti, etenkin parenteraalisesti annettavien valmisteiden aseptista käsittelyä koskevien ohjeiden mukaisesti.
- Käyttökuntoon saatettua laskimoon annettavaa infuusioliuosta säilytetään asianmukaisesti, jotta varmistetaan aseptisten olosuhteiden säilyminen.
Jos käyttökuntoon saatettua liuosta on tarkoitus säilyttää yli 24 tuntia ennen käyttöä, käyttökuntoon saattaminen ja laimentaminen on tehtävä laminaarivirtauskaapissa tai biologisessa suojakaapissa laskimoon annettavien lääkeaineiden turvallista käsittelyä koskevien tavanomaisten varotoimien mukaisesti.
Trazimera-injektiopullo, jonka sisältö on liuotettu aseptisesti injektionesteisiin käytettävään veteen (ei sisälly pakkaukseen), säilyy kemiallisesti ja fysikaalisesti stabiilina 48 tuntia 2 °C–8 °C:ssa. Liuos ei saa jäätyä.
Trazimera 150 mg kuiva-aine välikonsentraatiksi infuusionestettä varten, liuos
Asianmukaista aseptista tekniikkaa on käytettävä. Jokaisen Trazimera 150 mg ‑injektiopullon sisältö saatetaan käyttökuntoon 7,2 ml:lla steriiliä injektionesteisiin käytettävää vettä (ei sisälly pakkaukseen). Muiden liuottimien käyttöä käyttökuntoon saattamisessa on vältettävä. Näin saadaan 7,4 ml kerta-annokseen soveltuvaa liuosta, joka sisältää trastutsumabia noin 21 mg/ml. Neljän prosentin ylitäyttö varmistaa, että ilmoitettu 150 mg:n annos saadaan vedettyä jokaisesta injektiopullosta.
Trazimera 420 mg kuiva-aine välikonsentraatiksi infuusionestettä varten, liuos
Asianmukaista aseptista tekniikkaa on käytettävä. Jokaisen Trazimera 420 mg ‑injektiopullon sisältö saatetaan käyttökuntoon 20 ml:lla steriiliä injektionesteisiin käytettävää vettä (ei sisälly pakkaukseen). Muiden liuottimien käyttöä käyttökuntoon saattamisessa on vältettävä. Näin saadaan 20,6 ml kerta-annokseen soveltuvaa liuosta, joka sisältää trastutsumabia noin 21 mg/ml. Viiden prosentin ylitäyttö varmistaa, että ilmoitettu 420 mg:n annos saadaan vedettyä jokaisesta injektiopullosta.
|
Trazimera-injektiopullo
|
|
Steriilin injektionesteisiin käytettävän veden tilavuus
|
|
Lopullinen pitoisuus
|
|
150 mg:n injektiopullo
|
+
|
7,2 ml
|
=
|
21 mg/ml
|
|
420 mg:n injektiopullo
|
+
|
20 ml
|
=
|
21 mg/ml
|
Trazimera-valmistetta on käsiteltävä varoen käyttökuntoon saattamisen yhteydessä. Liiallinen vaahtoaminen käyttökuntoon saattamisen yhteydessä tai käyttökuntoon saatetun Trazimera-valmisteen ravistelu voi aiheuttaa ongelmia riittävän määrän vetämisessä injektiopullosta.
Ohjeet aseptiseen käyttökuntoon saattamiseen
- Käytä steriiliä ruiskua ja injisoi hitaasti asianmukainen tilavuus (ks. edellä) steriiliä injektionesteisiin käytettävää vettä kylmäkuivattua Trazimera-valmistetta sisältävään injektiopulloon.
- Pyöritä injektiopulloa varovaisesti käyttökuntoon saattamisen edistämiseksi. ÄLÄ RAVISTELE!
Pieni vaahtoaminen käyttökuntoon saattamisen yhteydessä ei ole poikkeuksellista. Anna injektiopullon seistä rauhassa noin 5 minuuttia. Käyttökuntoon saatettu Trazimera on väritön tai vaaleanrusehtavan keltainen, läpinäkyvä liuos, jossa ei saa olla näkyviä hiukkasia.
Tarvittava liuostilavuus lasketaan seuraavasti:
- Aloitusannos 4 mg/kg trastutsumabia ja viikoittainen ylläpitoannos 2 mg/kg trastutsumabia:
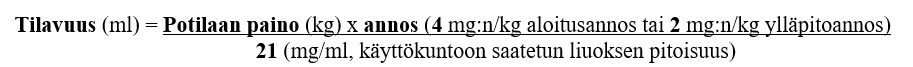
- Aloitusannos 8 mg/kg trastutsumabia ja 3 viikon välein annettava ylläpitoannos 6 mg/kg trastutsumabia:

Tarvittava määrä konsentraattia vedetään injektiopullosta käyttäen steriiliä neulaa ja ruiskua ja lisätään polyvinyylikloridista, polyeteenistä, polypropeenista tai etyleenivinyyliasetaatista valmistettuun infuusiopussiin tai lasiseen infuusiopulloon, jossa on 250 ml 9 mg/ml (0,9 %) natriumkloridi-injektioliuosta. Älä käytä glukoosia sisältäviä liuoksia. Liuosta sekoitetaan kääntelemällä pussia tai pulloa varovaisesti ylösalaisin, jotta vältytään liuoksen vaahtoamiselta. Parenteraaliset liuokset on ennen annostelua tarkastettava silmämääräisesti mahdollisten partikkeleiden tai värimuutosten varalta.