Movymia 20 mikrogrammaa/80 mikrolitrassa, injektioneste, liuos
teriparatidi
Yleisiä ohjeita
Lue tämä pakkausseloste huolellisesti ennen kuin aloitat tämän lääkkeen käyttämisen, sillä se sisältää sinulle tärkeitä tietoja.
- Säilytä tämä pakkausseloste. Voit tarvita sitä myöhemmin.
- Jos sinulla on kysyttävää, käänny lääkärin tai apteekkihenkilökunnan puoleen.
- Tämä lääke on määrätty vain sinulle eikä sitä pidä antaa muiden käyttöön. Se voi aiheuttaa haittaa muille, vaikka heillä olisikin samanlaiset oireet kuin sinulla.
- Jos havaitset haittavaikutuksia, kerro niistä lääkärille tai apteekkihenkilökunnalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Ks. kohta Mahdolliset haittavaikutukset.
Tässä pakkausselosteessa kerrotaan
1. Mitä Movymia on ja mihin sitä käytetään
2. Mitä sinun on tiedettävä, ennen kuin käytät Movymia-valmistetta
3. Miten Movymia-valmistetta käytetään
4. Mahdolliset haittavaikutukset
5. Movymia-valmisteen säilyttäminen
6. Pakkauksen sisältö ja muuta tietoa
1. Mitä valmiste on ja mihin sitä käytetään
Movymia sisältää vaikuttavana aineena teriparatidia, joka vahvistaa luuta ja vähentää murtumavaaraa edistämällä luun muodostusta.
Movymia on tarkoitettu aikuisten osteoporoosin hoitoon. Osteoporoosi on sairaus, joka aiheuttaa luiden ohenemista ja haurastumista. Tämä tauti on erityisen yleinen vaihdevuosi-iän ohittaneilla naisilla, mutta sitä voi ilmetä myös miehillä. Osteoporoosia esiintyy myös usein potilailla, jotka käyttävät kortikosteroideiksi kutsuttuja lääkkeitä.
2. Mitä sinun on tiedettävä ennen valmisteen käyttöä
Älä käytä Movymia-valmistetta
• jos olet allerginen teriparatidille tai tämän lääkkeen jollekin muulle aineelle (lueteltu kohdassa Pakkauksen sisältö ja muuta tietoa)
• jos veresi kalsiumpitoisuus on suuri (sinulla on ennestään hyperkalsemia).
• jos sinulla on vakavia munuaisvaivoja.
• jos sinulla on milloinkaan ollut luusyöpä tai muu syöpä, joka on levinnyt luustoon (etäpesäkkeitä luustossa).
• tiettyjen luusairauksien yhteydessä. Jos sinulla on jokin luuston sairaus, kerro se lääkärillesi.
• jos sinulla on selittämätön, suurentunut alkalisen fosfataasin arvo. Tämä voi viitata sinulla mahdollisesti olevaan Pagetin luutautiin (sairaus, jossa luun muodostuminen on häiriintynyt). Jos et ole varma, kysy lääkäriltäsi.
• jos olet saanut sädehoitoa luustoon.
• jos olet raskaana tai imetät.
Varoitukset ja varotoimet
Movymia voi lisätä kalsiumpitoisuutta veressä tai virtsassa.
Keskustele lääkärin kanssa ennen kuin käytät tai kun käytät Movymia-valmistetta:
• jos sinulla on jatkuvaa pahoinvointia, oksentelua, ummetusta, vetämättömyyttä tai lihasheikkoutta. Nämä voivat olla oireita veren liian suuresta kalsiumpitoisuudesta.
• jos sinulla on tai on ollut munuaiskiviä.
• jos sinulla on munuaisvaivoja (kohtalainen munuaisten vajaatoiminta).
Joillekin potilaille Movymia voi aiheuttaa huimausta tai sydämen tykytystä muutaman ensimmäisen pistoksen jälkeen. Ota Movymia-pistos ensimmäisillä kerroilla sellaisessa paikassa, että voit istua tai mennä pitkäksesi, jos saat huimausta.
Suositeltua 24 kuukauden hoitoaikaa ei pidä ylittää.
Kirjaa sylinteriampullin eränumero ja ensimmäisen pistoksen päivämäärä sylinteriampullin koteloon ennen kuin asetat sylinteriampullin Movymia Pen -injektiokynään, ja mainitse nämä tiedot ilmoittaessasi mahdollisista haittavaikutuksista.
Movymia-valmistetta ei tule antaa aikuisille, jotka voivat vielä kasvaa.
Lapset ja nuoret
Movymia-valmistetta ei tule antaa lapsille tai nuorille (alle 18-vuotiaille).
Muut lääkevalmisteet ja Movymia
Kerro lääkärille tai apteekkihenkilökunnalle, jos parhaillaan käytät olet äskettäin käyttänyt tai saatat käyttää muita lääkkeitä.
Tämä on tärkeää, koska joillain lääkkeillä (esim. digoksiini/digitalis -valmisteet, joita käytetään sydäntaudeissa) voi olla yhteisvaikutuksia teriparatidin kanssa.
Raskaus ja imetys
Älä käytä Movymia-valmistetta, jos olet raskaana tai imetät. Jos olet hedelmällisessä iässä oleva nainen, sinun on käytettävä luotettavaa raskauden ehkäisymenetelmää Movymia-lääkityksen aikana. Jos tulet raskaaksi käyttäessäsi Movymiaa, Movymia on lopetettava. Kysy lääkäriltä tai apteekista neuvoa ennen tämän lääkkeen käyttöä.
Ajaminen ja koneiden käyttö
Joillekin potilaille Movymia-pistos voi aiheuttaa huimausta. Jos sinua huimaa, älä aja autoa äläkä käytä koneita ennen kuin olosi paranee.
Movymia sisältää natriumia
Tämä lääkevalmiste sisältää alle 1 mmol natriumia (23 mg) per annos eli sen voidaan sanoa olevan ”natriumiton”.
3. Miten valmistetta käytetään
Käytä tätä lääkettä juuri siten kuin lääkäri on määrännyt. Tarkista ohjeet lääkäriltä tai apteekista, jos olet epävarma.
Suositeltu annos on 20 mikrogrammaa (vastaa 80 mikrolitraa) kerran vuorokaudessa pistoksena ihon alle (ihonalainen injektio) reiteen tai vatsan alueelle.
Jotta muistat käyttää lääkettäsi, pistä se suunnilleen samaan aikaan joka päivä. Movymia voidaan pistää ruokailun yhteydessä. Ota Movymia-pistos joka päivä niin pitkään kuin lääkärisi on sinulle määrännyt. Movymia-hoidon kesto on enintään 24 kuukautta. Voit saada elinaikanasi vain yhden 24 kuukauden Movymia-hoidon.
Lääkärisi voi määrätä sinulle Movymia-pistoksen lisäksi kalsium- ja D-vitamiinilisiä. Lääkärisi kertoo sinulle, kuinka paljon kalsiumia ja D-vitamiinia voit ottaa päivässä.
Movymia voidaan ottaa ruokailun yhteydessä tai ilman ruokaa.
Movymia-sylinteriampullit on suunniteltu käytettäväksi ainoastaan uudelleenkäytettävällä usean annoksen Movymia Pen -injektiokynällä ja yhteensopivilla injektioneuloilla. Injektiokynä ja neulat eivät sisälly Movymia-lääkepakkaukseen. Hoito tulisi aloittaa käyttämällä sylinteriampulli- ja injektiokynäpakkausta, joka sisältää yhden Movymia-sylinteriampullin sisäkotelon ja yhden Movymia Pen -injektiokynänn sisäkotelon.
Injektiokynän kanssa voidaan käyttää injektioneuloja, joiden ISO-standardin mukainen koko on 29 – 31 G (halkaisija 0,25–0,33 mm) ja pituus 5–12,7 mm ja jotka on tarkoitettu vain ihonalaista injektiota varten.
Aseta sylinteriampulli injektiokynään ennen ensimmäistä käyttökertaa. On lääkkeen oikean käytön vuoksi erittäin tärkeää, että noudatat tarkasti injektiokynän mukana toimitettavia käyttöohjeita.
Käytä kullakin pistokerralla uutta injektioneulaa tartunnan estämiseksi, ja hävitä neula turvallisesti käytön jälkeen.
Älä koskaan säilytä injektiokynää niin, että neula on siinä kiinni.
Älä koskaan anna muiden käyttää injektiokynääsi.
Älä käytä Movymia Pen -injektiokynää muiden lääkkeiden (esim. insuliinin) pistämiseen.
Injektiokynä on suunniteltu käytettäväksi ainoastaan Movymian kanssa.
Älä täytä sylinteriampullia uudelleen.
Älä siirrä lääkettä injektioruiskuun.
Pistä Movymia pian sen jälkeen, kun olet ottanut injektiokynän ja siihen asetetun sylinteriampullin jääkaapista. Pane injektiokynä ja siihen asetettu sylinteriampulli takaisin jääkaappiin heti käytön jälkeen. Älä irrota sylinteriampullia injektiokynästä jokaisen käyttökerran jälkeen. Säilytä sitä sylinteriampullin pidikkeessä koko 28 päivää kestävän hoitojakson ajan.
Injektiokynän valmistelu käyttöön
- Lue aina Movymia Pen -injektiokynän käyttöohjeet, jotka löytyvät injektiokynän kotelosta, jotta osaat antaa Movymian oikein.
- Pese kätesi ennen kuin käsittelet sylinteriampullia tai injektiokynää.
- Tarkista sylinteriampullin etikettiin merkitty viimeinen käyttöpäivämäärä ennen sylinteriampullin asettamista injektiokynään. Varmista, että sen viimeiseen käyttöpäivään on vähintään 28 päivää. Aseta sylinteriampulli injektiokynään ennen ensimmäistä käyttökertaa injektiokynän ohjeiden mukaisesti. Kirjaa kunkin sylinteriampullin eränumero ja ensimmäisen pistoksen päivämäärä kalenteriin. Ensimmäisen pistoksen päivämäärä on kirjoitettava myös Movymia-koteloon (ks. pakkauksen kohta: {Ensimmäinen käyttökerta:}).
- Kun olet asettanut uuden sylinteriampullin, viritä injektiokynä toimitettujen ohjeiden mukaisesti ennen ensimmäistä pistosta. Älä viritä injektiokynää uudelleen ensimmäisen annoksen jälkeen.
Movymian pistäminen
- Puhdista pistokohdan iho (reisi tai vatsa) ennen Movymia-pistosta lääkärisi antamien ohjeiden mukaisesti.
- Nipistä puhdistettua ihoa kevyesti poimulle ja työnnä neula suoraan ihoon. Paina painiketta ja pidä sitä painettuna, kunnes annosilmaisin on palannut alkuasentoon.
- Anna neulan olla pistoksen jälkeen kuuden sekunnin ajan ihossa, jotta saat koko annoksen.
- Aseta neulan ulkosuojus injektiokynän neulan päälle välittömästi pistoksen jälkeen ja kierrä suojusta vastapäivään neulan irrottamiseksi. Näin jäljelle jäänyt Movymia pysyy steriilinä, eikä vuoda injektiokynästä. Sylinteriampulliin ei myöskään pääse ilmaa, eikä neula tukkeennu.
- Aseta suojus takaisin injektiokynän päälle. Jätä sylinteriampulli injektiokynään.
Jos otat enemmän Movymia-valmistetta kuin sinun pitäisi
Jos olet vahingossa ottanut enemmän Movymia-lääkettä kuin olisi pitänyt, ota yhteyttä lääkäriin tai apteekkiin. Yliannostuksen odotettuja oireita ovat pahoinvointi, oksentelu, heitehuimaus ja päänsärky.
Jos unohdat käyttää Movymia-valmistetta
Jos unohdat ottaa pistoksen tai et pysty ottamaan lääkettä tavanomaiseen aikaan, pistä se mahdollisimman pian saman päivän aikana. Älä ota kaksinkertaista annosta korvataksesi unohtamasi kerta-annoksen. Ota vain yksi pistos päivässä.
Jos lopetat Movymia-valmisteen käytön
Jos harkitset Movymian käytön lopettamista, keskustele asiasta lääkärisi kanssa. Lääkärisi neuvoo sinua ja päättää Movymia-lääkityksesi kestosta.
Jos sinulla on kysymyksiä tämän lääkkeen käytöstä, käänny lääkärin tai apteekkihenkilökunnan puoleen.
4. Mahdolliset haittavaikutukset
Kuten kaikki lääkkeet, tämäkin lääke voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa.
Yleisimpiä haittavaikutuksia ovat raajoissa ilmenevä kipu (hyvin yleinen, voi esiintyä yli 1 potilaalla 10:stä). Muita yleisiä haittavaikutuksia (esiintyy enintään 1 potilaalla 10:stä) ovat huonovointisuus, päänsärky ja heitehuimaus. Jos sinua alkaa huimata pistoksen ottamisen jälkeen, istu tai asetu makuulle, kunnes olosi paranee. Jos olosi ei parane, soita lääkärille ennen hoidon jatkamista. Teriparatidin käytön jälkeen on esiintynyt pyörtymistapauksia.
Joillakin voi olla oireilua pistoskohdassa, kuten ihon punoitusta, kipua, turvotusta, kutinaa, mustelma tai vähäistä verenvuotoa pistosalueella (joita esiintyy yleisesti). Niiden pitäisi hävitä muutamassa päivässä tai viikossa. Jos näin ei tapahdu, kerro asiasta lääkärillesi.
Harvinaisissa tapauksissa (voi esiintyä enintään 1 potilaalla 1 000:sta) potilailla voi ilmetä yliherkkyysoireita kuten hengitysvaikeuksia, kasvojen turvotusta, ihottumaa ja rintakipua. Nämä oireet ilmaantuvat tavallisesti pian pistoksen jälkeen. Harvinaisissa tapauksissa voi esiintyä vakavia ja mahdollisesti henkeä uhkaavia allergisia reaktioita, kuten anafylaksiaa.
Muita haittavaikutuksia:
Yleiset (voi esiintyä enintään 1 potilaalla 10:stä)
• veren kolesterolipitoisuuden suurentuminen
• masennus
• hermosärkyä jaloissa
• pyörryttäminen
• huimaus
• epäsäännölliset sydämenlyönnit
• hengenahdistus
• lisääntynyt hikoilu
• lihaskouristukset
• vetämättömyys
• väsymys
• rintakipu
• matala verenpaine
• närästys (kipeä tai polttava tunne rintalastan alla)
• oksentelu
• ruokatorven tyrä (palleatyrä)
• matala hemoglobiini eli punasolujen määrä (anemia)
Melko harvinaiset (voi esiintyä enintään 1 potilaalla 100:sta)
• sykkeen kiihtyminen
• epätavallinen sydänääni
• hengästyminen
• peräpukamat
• virtsan karkaaminen
• lisääntynyt virtsaamistarve
• painon nousu
• munuaiskivet
• lihas- ja nivelkipu. Joillakin potilailla on ollut vaikeita selkälihaskouristuksia (kramppeja) tai kipua, jotka ovat vaatineet sairaalahoitoa.
• suurentunut veren kalsiumpitoisuus
• suurentunut veren virtsahappopitoisuus
• alkalinen fosfataasi -nimisen entsyymin (AFOS) arvon suurentumista
Harvinaiset (voi esiintyä enintään 1 potilaalla 1 000:sta)
• eriasteinen munuaisten vajaatoiminta
• turvotus lähinnä käsissä, jalkaterissä ja säärissä
Haittavaikutuksista ilmoittaminen
Jos havaitset haittavaikutuksia, kerro niistä lääkärille tai apteekkihenkilökunnalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Voit ilmoittaa haittavaikutuksista myös suoraan liitteessä V luetellun kansallisen ilmoitusjärjestelmän kautta. Ilmoittamalla haittavaikutuksista voit auttaa saamaan enemmän tietoa tämän lääkevalmisteen turvallisuudesta.
5. Valmisteen säilyttäminen
Ei lasten ulottuville eikä näkyville.
Älä käytä tätä lääkettä pakkauksessa mainitun viimeisen käyttöpäivämäärän (EXP) jälkeen. Viimeinen käyttöpäivämäärä tarkoittaa kuukauden viimeistä päivää.
Säilytä jääkaapissa (2 °C – 8 °C). Ei saa jäätyä.
Säilytä sylinteriampullia kotelossa suojassa valolta.
Movymia-valmistetta voidaan käyttää enintään 28 päivän ajan ensimmäisen pistokerran jälkeen, jos sylinteriampullia/injektiokynää ja siihen asetettua sylinteriampullia on säilytetty jääkaapissa (2 °C − 8 °C).
Älä pane sylinteriampullia jääkaapin pakastelokeron lähelle, jotta se ei jäädy. Älä käytä Movymia-valmistetta, jos se on jäätynyt.
Jokainen sylinteriampulli tulee hävittää asianmukaisesti 28 päivän kuluttua ensimmäisestä käyttökerrasta, vaikka se ei olisi täysin tyhjä.
Movymia sisältää väritöntä ja kirkasta liuosta. Älä käytä Movymiaa, jos liuoksessa on kiinteitä hiukkasia tai jos se on samea tai värjäytynyt.
Lääkkeitä ei pidä heittää viemäriin eikä hävittää talousjätteiden mukana. Kysy käyttämättömien lääkkeiden hävittämisestä apteekista. Näin menetellen suojelet luontoa.
6. Pakkauksen sisältö ja muuta tietoa
Mitä Movymia sisältää
- Vaikuttava aine on teriparatidi. Yksi 80 mikrolitran annos sisältää 20 mikrogrammaa teriparatidia. Yksi 2,4 ml sylinteriampulli sisältää 600 mikrogrammaa teriparatidia (vastaa 250 mikrogrammaa/ml).
- Muut aineet ovat väkevä etikkahappo, mannitoli, metakresoli, natriumasetaattitrihydraatti, kloorivetyhappo (happamuuden säätöön), natriumhydroksidi (happamuuden säätöön) ja injektionesteisiin käytettävä vesi (ks. kohta Mitä sinun on tiedettävä ennen valmisteen käyttöä ”Movymia sisältää natriumia”).
Lääkevalmisteen kuvaus ja pakkauskoot
Movymia on väritön ja kirkas injektioneste, liuos (injektio). Se toimitetaan sylinteriampullissa. Yksi sylinteriampulli sisältää 2,4 ml liuosta, josta riittää 28 annokseen.
Pakkauskoot: 1 sylinteriampulli tai 3 sylinteriampullia pakattuna foliokannella suljettuun muoviastiaan ja pakattuna koteloon.
Movymian sylinteriampulli- ja injektiokynäpaketti: 1 Movymia-sylinteriampulli, joka on pakattu foliokannella suljettuun muoviastiaan ja sisäkoteloon, ja 1 Movymia Pen -injektiokynä, joka on pakattu sisäkoteloon.
Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
Myyntiluvan haltija
STADA Arzneimittel AG
Stadastrasse 2-18
61118 Bad Vilbel
Saksa
Valmistaja
Gedeon Richter Plc.
Gyömrői út 19-21.
1103 Budapest
Unkari
STADA Arzneimittel AG
Stadastrasse 2–18
61118 Bad Vilbel
Saksa
Lisätietoja tästä lääkevalmisteesta antaa myyntiluvan haltijan paikallinen edustaja.
Suomi/Finland
STADA Nordic ApS, Suomen sivuliike
Puh/Tel: +358 207416888
Tämä pakkausseloste on tarkistettu viimeksi 7.5.2025
Muut tiedonlähteet
Lisätietoa tästä lääkevalmisteesta on saatavilla Euroopan lääkeviraston verkkosivulla https://www.ema.europa.eu /
Tästä valmisteesta saa ysityiskohtaista tietoa myös lukemalla alla tai kotelossa olevan QR‑koodin älypuhelimella. Samat tiedot ovat saatavilla myös seuraavassa osoitteessa: movymiapatients.com
Ohjeet käyttäjälle
Movymia Pen
Toistokäyttöinen injektiokynä käytettäväksi Movymia-sylinteriampullien kanssa ihonalaisiin pistoksiin
Noudata aina alla ja takasivulla annettuja ohjeita, kun käytät Movymia Pen –injektiokynää.
Movymia Pen -injektiokynän osat
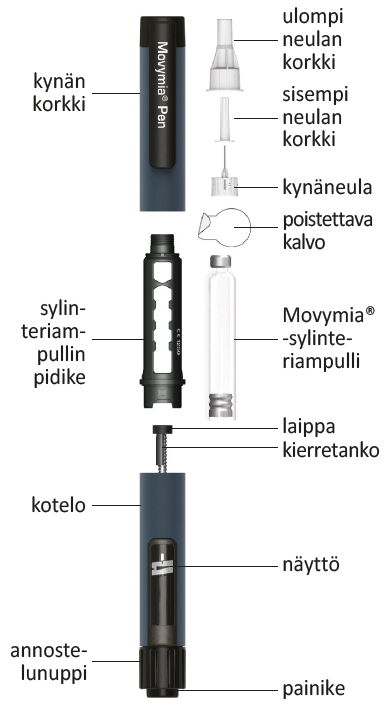
Kynän valmistelu – Ensimmäinen käyttökerta / sylinteriampullin vaihto
Merkitse muistiin uuden sylinteriampullin ensimmäinen käyttöpäivä. Näin tiedät, milloin sylinteriampullin 28 päiväannosta on käytetty (ks. kohta Mitä sinun on tiedettävä ennen valmisteen käyttöä ”Varoitukset ja varotoimet” ja kohta Miten valmistetta käytetään ”Injektiokynän valmistelu käyttöön” Movymia-valmisteen pakkausselosteesta).
Noudata ohjeita aina, kun asetat uuden Movymia-sylinteriampullin Movymia Pen -injektiokynääsi. Älä tee tätä ennen jokaista päivittäistä pistosta, koska silloin Movymia ei riitä 28 päiväksi.
Lue erillinen Movymia-sylinteriampullin potilastietoesite.
A: Poista injektiokynän korkki.
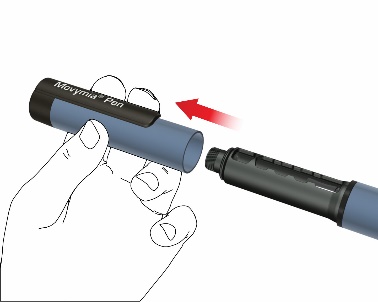
B: Poista sylinteriampullin pidike kääntämällä sitä (pikaliitin).
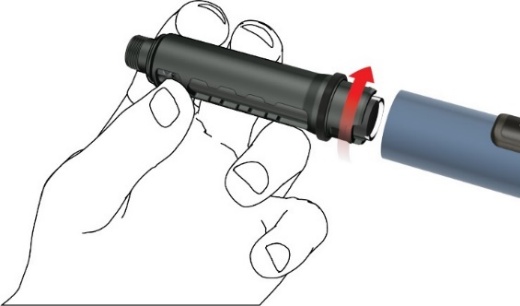
C: Poista tyhjä sylinteriampulli, jos olet vaihtamassa sylinteriampullia. Aseta uusi Movymia-sylinteriampulli ampullipidikkeeseen niin, että sylinteriampullin metallikorkki menee ensin.
D: Paina kierretanko varovasti suorassa takaisin sormellasi niin pitkälle kuin se menee. Tämä ei ole tarpeen silloin, kun tanko on alkuasennossa, kuten esimerkiksi ensimmäisellä käyttökerralla. Kierretankoa ei voi työntää kynän koteloon kokonaan.
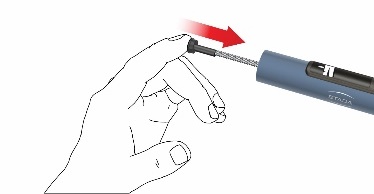
E: Kiinnitä sylinteriampullin pidike koteloon kiertämällä sitä 90 astetta, kunnes se pysähtyy.
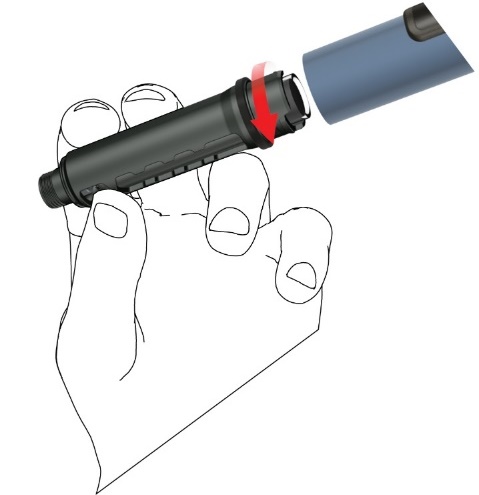
F: Kiinnitä uusi kynäneula seuraavalla tavalla:
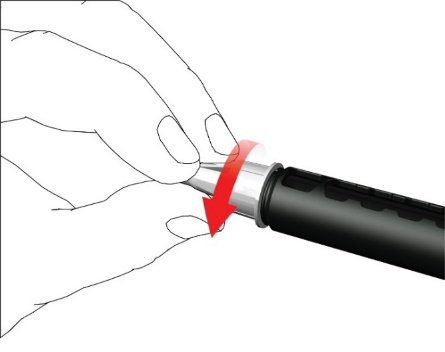
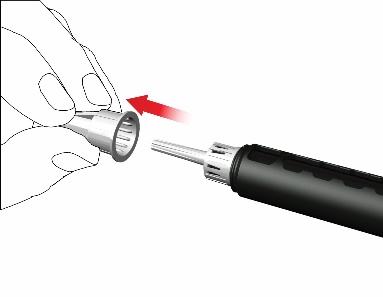
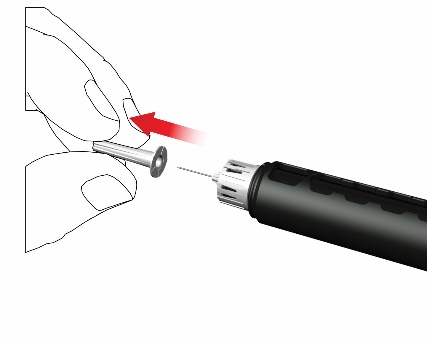
- Poista kalvo.
- Kierrä kynäneula myötäpäivään kiinni sylinteriampullin koteloon. Varmista, että kynäneula on oikein ja tukevasti kiinni sylinteriampullin pidikkeessä.
- Poista neulan ulompi korkki ja säästä se.
- Poista neulan sisempi korkki ja heitä se pois.
Kun kiinnität neulaa, muutamia pisaroita voi karata. Se on täysin normaalia.
G: Valmistelu
Kynä tulee valmistella ja testata aina, kun siihen on asetettu uusi sylinteriampulli, ennen kuin ampullilla tehdään ensimmäinen pistos.
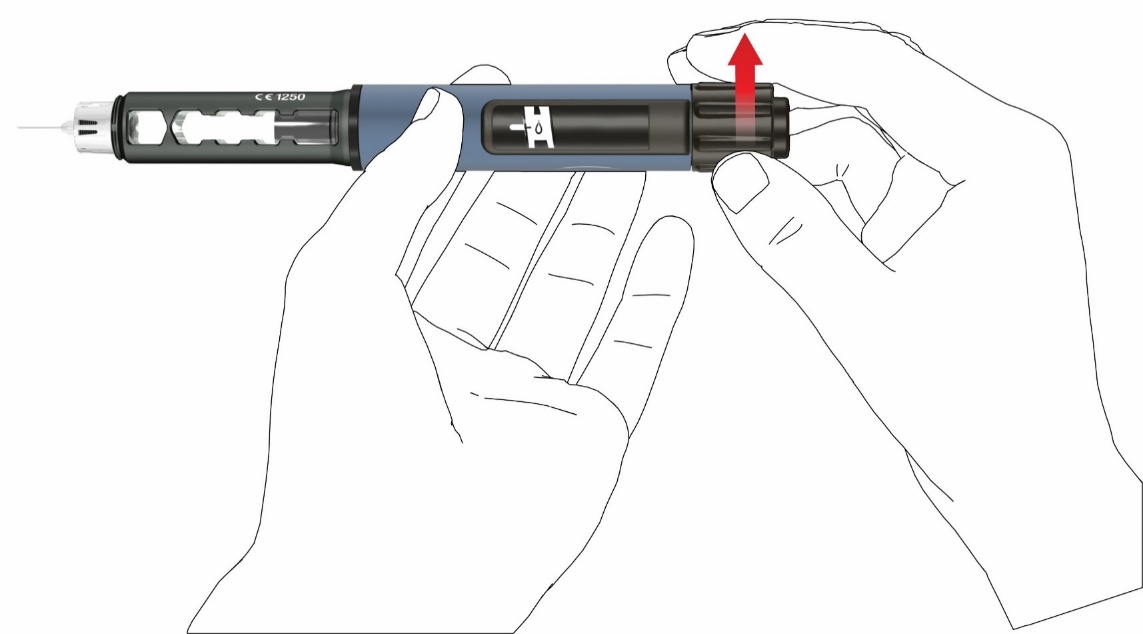
- Käännä annostelunuppia myötäpäivään, kunnes näet pisaramerkin näytöllä. Varmista, että kaksi merkkiviivaa on kohdistettu. Kun kierrät kynää annostellaksesi lääkkeen, siitä kuuluu selvä napsahdus ja siinä on selvä vastus.
- Pidä kynää niin, että neula osoittaa ylöspäin.
- Paina painike täysin sisään. Paina sitä, kunnes annosilmaisin on taas alkutilassa. Muutama pisara lääkettä tulee valua pois neulan kärjestä.
Jos pisaroita ei ilmesty, toista kohta G, kunnes näet niitä. Älä toista kohtaa G enempää kuin neljä kertaa, vaan noudata ohjeita Vianmääritys-osassa takasivulla.
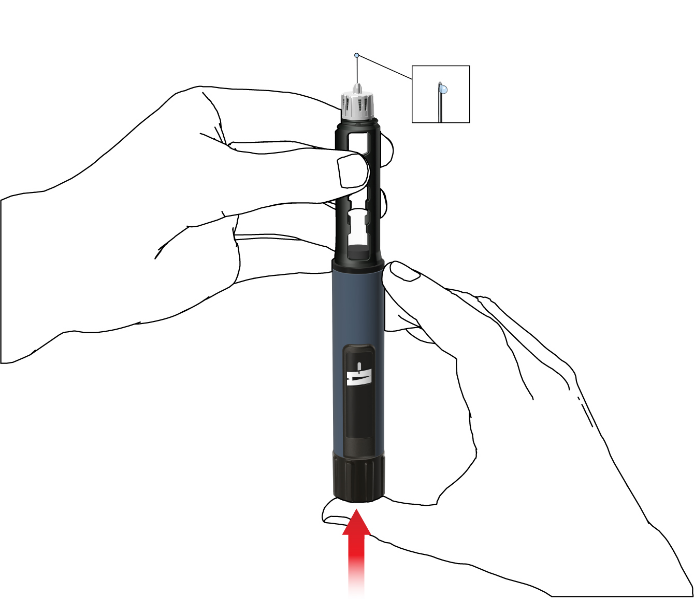
Lääkkeen antaminen Movymia Pen -injektiokynällä
Pese kätesi huolellisesti saippualla infektioriskin pienentämiseksi.
Varmista, että sinulla on valmiina:
- Movymia Pen -injektiokynä, jossa on sylinteriampulli
- sopiva kynäneula
- pistonkestävä teräville esineille tarkoitettu roska-astia käytetyille neuloille.
Älä käytä injektiokynää, jos sylinteriampulli näyttää samealta, vääränväriseltä tai siinä on hiukkasia.
Lue erillinen Movymia-sylinteriampullin potilastietoesite.
1. Kiinnitä kynäneula
Käytä uutta neulaa jokaiseen pistokseen. Älä käytä kynäneulaa, jos pakkaus on vahingoittunut tai et ole avannut sitä itse.
Huomautus: Sinun ei tarvitse vaihtaa neulaa, kun käytät injektiokynää heti valmistelun jälkeen. Tässä tapauksessa jatka kohdasta ”2. Annoksen asettaminen ja pistäminen”.
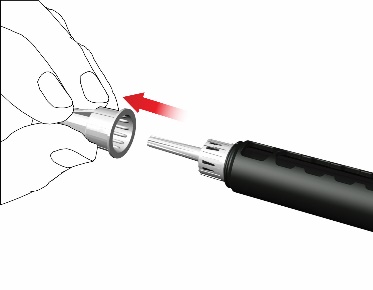
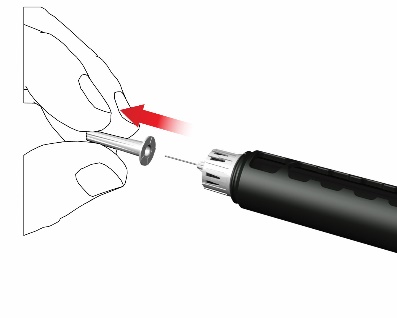
- Poista kalvo.
- Kierrä kynäneula myötäpäivään kiinni sylinteriampullin koteloon. Varmista, että kynäneula on oikein ja tukevasti kiinni sylinteriampullin pidikkeessä.
- Poista neulan ulompi korkki ja säästä se.
- Poista neulan sisempi korkki ja heitä se pois.
Kun kiinnität neulaa, muutamia pisaroita voi karata. Se on täysin normaalia.
2. Annoksen asettaminen ja pistäminen
Varoitus: Varmista, että käytössäsi on oikea lääke. Tarkista sylinteriampullin nimike, ennen kuin asetat sen ampullipidikkeeseen.
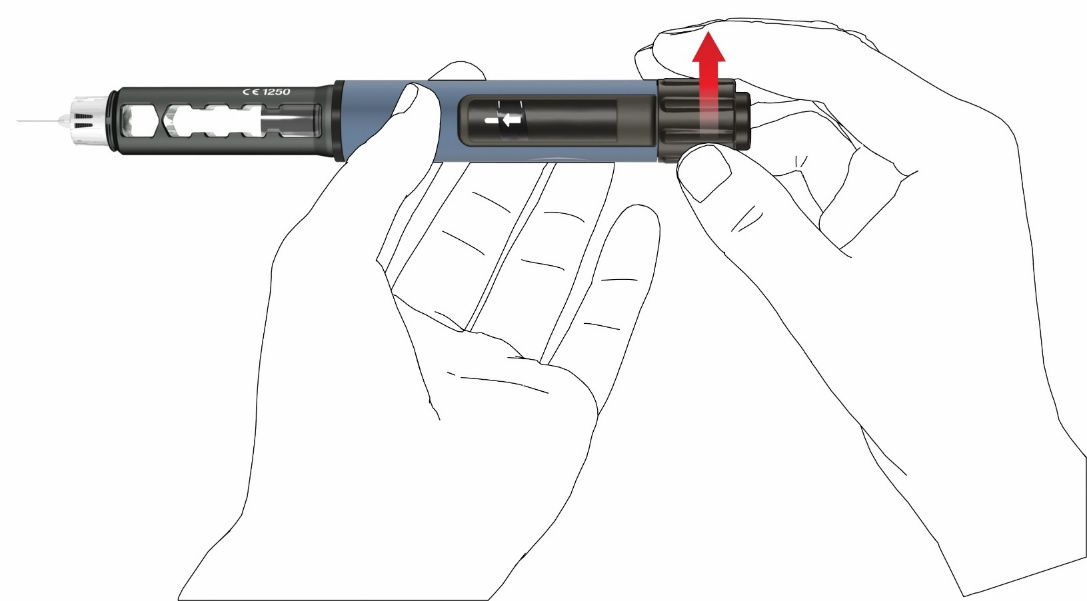
- Asettaaksesi päivittäisen 80 mikrolitran annoksen käännä annostelunuppia myötäpäivään, kunnes se pysähtyy, eikä sitä voi enää kääntää. Varmista, että näytössä näkyy nuolimerkki ja se on kohdakkain merkkiviivan kanssa. Kun kierrät kynää annostellaksesi lääkkeen, siitä kuuluu selvä napsahdus ja siinä on selvä vastus. Älä yritä kääntää annostelunuppia pidemmälle väkisin.
Huomautus: Jos sylinteriampullissa on alle 80 mikrolitraa jäljellä, annostelunuppia ei voi kääntää myötäpäivään nuolimerkille. Tässä tapauksessa poista kynäneula, vaihda sylinteriampulli ja suorita valmistelu injektiokynän valmistelukohtien mukaan.
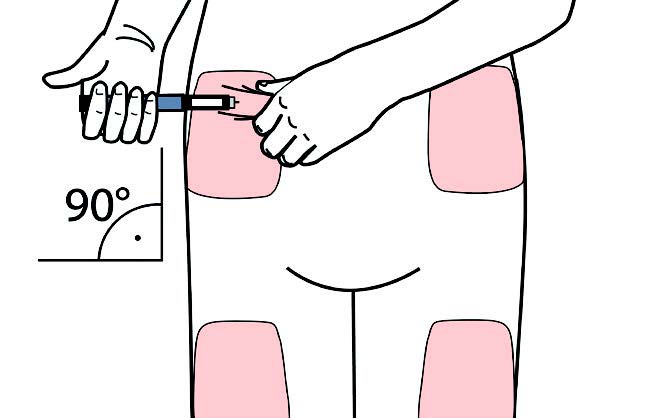
- Valitse sopiva paikka pistokselle ja valmistele ihosi lääkärisi neuvomalla tavalla. Pidä ihopoimua hellävaroen peukalon ja etusormen välissä. Pistä neula suoraan ja varovasti ihoon havaintokuvan mukaisesti.
Varoitus: Estä kynäneulaa taipumasta tai rikkoutumasta. Älä kallista kynää sen jälkeen, kun neula on ihossa. Kynän kallistaminen saattaa taivuttaa tai rikkoa neulan. Rikkinäiset neulat voivat jäädä kiinni ihoon. Jos rikkinäinen neula jää kiinni ihoon, ota heti yhteyttä lääkäriin.
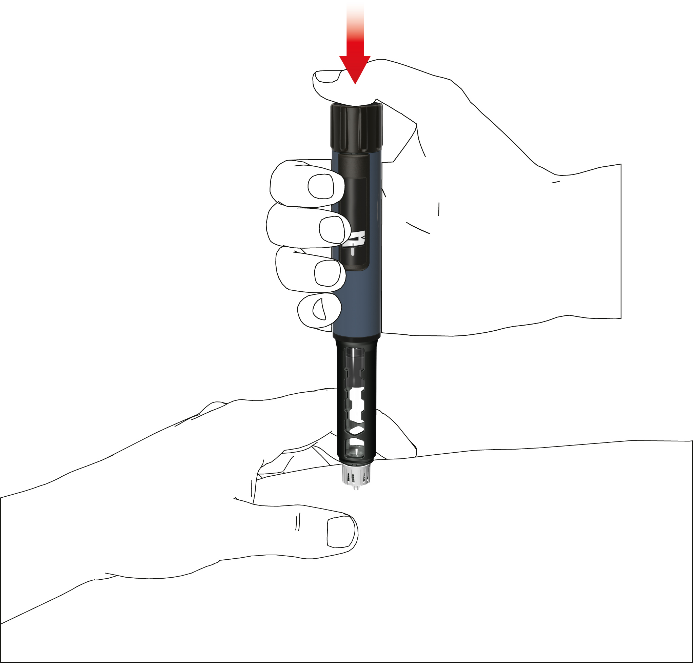
- Paina painiketta, kunnes annosilmaisin on palannut alkutilaan. Pidä neulaa ihopoimussa vielä kuusi sekuntia.
- Vedä kynä hitaasti pois. Tarkista, että näyttö on aloitusasennossa, jotta koko annos on varmasti pistetty.
3. Kynäneulan poistaminen
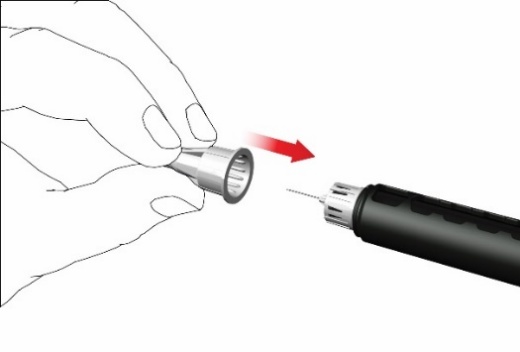
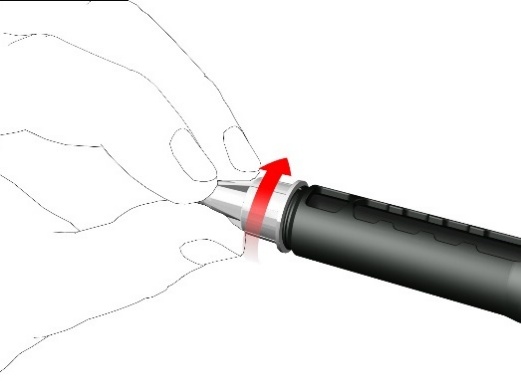
- Kiinnitä varovasti ulompi neulan korkki kynäneulaan.
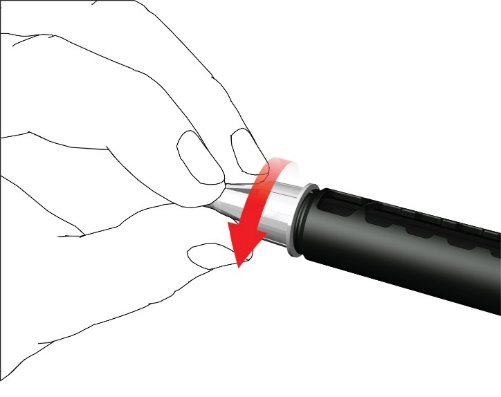
- Kierrä neulan korkkia vastapäivään, jotta saat poistettua kynäneulan. Hävitä se asianmukaisesti esimerkiksi pistonkestävässä teräville esineille tarkoitetussa roska-astiassa.
4. Sulje injektiokynän korkki uudelleen
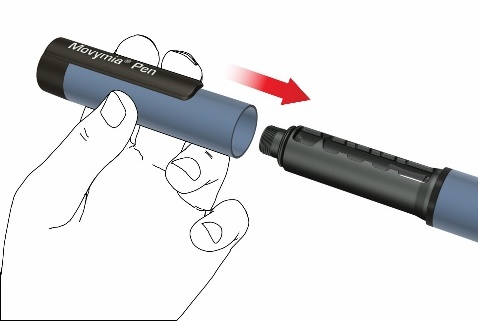
- Älä poista sylinteriampullia Movymia Pen -injektiokynästä, ennen kuin se on tyhjä.
- Sulje injektiokynän korkki jokaisen käytön jälkeen.
- Aseta Movymia Pen -injektiokynä, jossa on sylinteriampulli, takaisin lämpötilaltaan 2–8 °C:n jääkaappiin heti käytön jälkeen.
Huomautus terveydenhuollon ammattilaisille
Paikalliset terveydenhuollon ammattilaisten tai laitosten säännöt saattavat korvata tässä esitetyt ohjeet koskien neulan käsittelyä ja hävittämistä.
Lisätietoja
Uudelleenkäytettävä tietyn kokoisia annoksia sisältävä injektiokynä on suunniteltu, jotta osteoporoosin hoitaminen Movymialla olisi mahdollisimman helppoa. Jokaisessa Movymia-sylinteriampullissa on 28 annosta, joista jokainen sisältää 80 mikrolitraa Movymiaa.
Käytä Movymia-injektiokynääsi vain lääkärisi määräämällä tavalla sekä näiden käyttöohjeiden ja Movymia-pakkausesitteen mukaisesti.
Movymia Pen -injektiokynää voivat käyttää yli 18-vuotta täyttäneet potilaat, jotka hoitavat pistämisen itse, terveydenhoitoalan ammattilaiset ja kolmannet osapuolet, kuten täysi-ikäiset sukulaiset.
Sokea tai näkörajoitteinen potilas ei saa käyttää Movymia Pen -injektiokynää ilman apua koulutetulta ja pystyvältä henkilöltä. Käänny lääkärin puoleen, jos sinulla on kuulo- tai käsittelyongelmia.
Kynäneuloja tulee käyttää vain kerran, ja Movymia-sylinteriampullia saa käyttää vain yksi henkilö.
Movymia Pen -injektiokynän säilyttäminen ja huolto
- Käsittele injektiokynääsi varoen. Älä pudota injektiokynää ja vältä sen osumista koviin pintoihin. Suojaa se vedeltä, pölyltä ja kosteudelta.
- Kostea pyyhe riittää Movymia Pen -injektiokynän puhdistamiseen. Älä käytä alkoholia, muita liuottimia tai puhdistusaineita. Älä koskaan upota Movymia Pen -injektiokynää veteen, sillä se voi vahingoittaa kynää.
- Älä käytä Movymia Pen -injektiokynää, jos se on vaurioitunut tai jos olet epävarma siitä, toimiiko se oikein.
- Kuljeta ja säilytä Movymia Pen -injektiokynää, jossa on sylinteriampulli, Movymian erillisessä pakkausesitteessä kerrotussa lämpötilassa.
- Säilytä Movymia Pen -injektiokynä, sylinteriampullit ja kynäneulat poissa lasten ulottuvilta.
- Älä koskaan säilytä Movymia Pen -injektiokynää neula kiinnitettynä, sillä tällöin kynänsäiliöön voi muodostua ilmakuplia.
Movymia Pen -injektiokynän ja käytettyjen lisävarusteiden hävittäminen
Movymia Pen -injektiokynän käyttöaika on kaksi vuotta. Ennen Movymia Pen -injektiokynän hävittämistä muista aina poistaa kynäneula ja sylinteriampulli. Neulat ja käytetyt sylinteriampullit tulee hävittää erikseen ja turvallisesti. Movymia Pen -injektiokynä voidaan hävittää paikallisten viranomaisten ohjeiden mukaisesti.
Varoitukset
Noudata näissä ohjeissa annettuja käyttöohjeita. Jos käyttöohjeita ei noudateta, vaarana on väärän lääkityksen tai annostuksen saaminen, tautien tarttuminen tai tulehdus. Pyydä heti apua terveydenhuoltoalan ammattilaiselta, jos olet huolissasi jostain.
Vianetsintä
Noudata taulukossa annettuja ohjeita, jos sinulla on kysyttävää Movymia Pen -injektiokynän käytöstä:
| Kysymys | Vastaus |
| Pieniä ilmakuplia näkyy sylinteriampullissa. | Pieni ilmakupla ei vaikuta annokseen eikä vahingoita sinua. |
| Neulaa ei voi kiinnittää. | Käytä toista neulaa. |
| Neula on poikki/käyrä/vääntynyt. | Käytä toista neulaa. |
| Injektiokynästä ei kuuluu selvää napsahdusta, kun käännät sitä annostusta varten. | Älä käytä injektiokynää. |
| Lääkettä ei tule neulasta ulos kynän valmistelun aikana kohdassa ”G: Valmistelu”. | Vaihda neula ja toista valmisteluprosessi, kuten on kuvattu kynän valmistelua kuvaavissa kohdissa ”F” ja ”G”. Jos lääkettä ei silti tule ulos, älä käytä kynää. |
| Annostelunuppia ei voi kääntää myötäpäivään nuolimerkille. | Movymiaa on sylinteriampullissa jäljellä alle 80 mikrolitraa. Vaihda sylinteriampulli, kynäneula ja suorita valmistelu kynän valmistelun mukaisesti. |
| Näyttö ei palaa alkuasentoon pistämisen jälkeen. | Älä pistä uudestaan saman päivän aikana. Käytä uutta neulaa pistosta varten seuraavana päivänä. Aseta annos ja pistä kohdan ”2. Annoksen asettaminen ja pistäminen” mukaan. Jos näyttö ei vieläkään palaa alkuasentoon pistoksen jälkeen, älä käytä injektiokynää. |
| Huomaat, että injektiokynä vuotaa. | Älä käytä injektiokynää. |
Annostelunuppi kääntyi vahingossa myötäpäivään, kun injektio oli annettu. Miten nollaan annostelunupin alkuasentoon? | Älä paina painiketta. Nollaa injektiokynä kääntämällä annostelunuppia vastapäivään aina alkuasentoon asti. |