Uusi kauppanimi: Prevenar 20 injektioneste, suspensio
konjugoitu pneumokokkipolysakkaridirokote (20-valenttinen, adsorboitu)
Lisäseuranta
▼Tähän lääkevalmisteeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti turvallisuutta koskevaa uutta tietoa. Voit auttaa ilmoittamalla kaikista mahdollisesti saamistasi haittavaikutuksista. Ks. kohdan Mahdolliset haittavaikutukset lopusta, miten haittavaikutuksista ilmoitetaan.
Yleisiä ohjeita
Lue tämä pakkausseloste huolellisesti ennen kuin saat tätä rokotetta, sillä se sisältää sinulle tärkeitä tietoja.
- Säilytä tämä pakkausseloste. Voit tarvita sitä myöhemmin.
- Jos sinulla on kysyttävää, käänny lääkärin, apteekkihenkilökunnan tai sairaanhoitajan puoleen.
- Tämä rokote on määrätty vain sinulle tai lapsellesi eikä sitä pidä antaa muiden käyttöön.
- Jos havaitset haittavaikutuksia, kerro niistä lääkärille, apteekkihenkilökunnalle tai sairaanhoitajalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Ks. kohta Mahdolliset haittavaikutukset.
Tässä pakkausselosteessa kerrotaan
1. Mitä Prevenar 20 on ja mihin sitä käytetään
2. Mitä sinun on tiedettävä, ennen kuin saat tai lapsesi saa Prevenar 20 -rokotetta
3. Miten Prevenar 20 -rokotetta annetaan
4. Mahdolliset haittavaikutukset
5. Prevenar 20 -rokotteen säilyttäminen
6. Pakkauksen sisältö ja muuta tietoa
1. Mitä valmiste on ja mihin sitä käytetään
Prevenar 20 on pneumokokkirokote, jota annetaan
- lapsille (iältään 6 viikosta 17 vuoteen) ehkäisemään sairauksia, kuten aivokalvotulehdusta (aivojen ympärille kehittyvä tulehdus), sepsistä (verenmyrkytystä) tai bakteremiaa (bakteereja verenkierrossa), keuhkokuumetta (keuhkotulehdus) ja korvatulehduksia (äkillinen välikorvatulehdus), joiden aiheuttajia ovat Streptococcus pneumoniae ‑bakteerin 20 tyyppiä
- 18 vuotta täyttäneille henkilöille ehkäisemään sairauksia, kuten keuhkokuumetta (keuhkotulehdus), sepsistä (verenmyrkytystä) tai bakteremiaa (bakteereja verenkierrossa) sekä aivokalvotulehdusta (aivojen ympärille kehittyvä tulehdus), joiden aiheuttajia ovat Streptococcus pneumoniae ‑bakteerin 20 tyyppiä.
Prevenar 20 suojaa 20:tä Streptococcus pneumoniae ‑bakteerityyppiä vastaan.
Rokote auttaa elimistöä tuottamaan omia vasta-aineita, jotka suojaavat sinua tai lastasi näitä sairauksia vastaan.
2. Mitä sinun on tiedettävä ennen valmisteen käyttöä
Prevenar 20 -rokotetta ei pidä antaa
- jos olet tai lapsesi on allerginen (yliherkkä) vaikuttaville aineille tai tämän lääkkeen jollekin muulle aineelle (lueteltu kohdassa Pakkauksen sisältö ja muuta tietoa) tai mille tahansa muulle kurkkumätätoksoidia sisältävälle rokotteelle.
Varoitukset ja varotoimet
Keskustele lääkärin, apteekkihenkilökunnan tai sairaanhoitajan kanssa ennen rokotusta, jos sinulla tai lapsellasi
- on parhaillaan tai on aiemmin Prevenar 20 -annoksen jälkeen ollut terveysongelmia, kuten allerginen reaktio tai hengitysvaikeus
- on vaikea-asteinen sairaus tai korkeaa kuumetta. Lievä kuume tai ylähengitystieinfektio (esim. nuhakuume) eivät kuitenkaan vaadi rokotuksen siirtämistä.
- on verenvuoto-ongelmia tai saat, tai lapsesi saa, herkästi mustelmia
- on heikentynyt immuunijärjestelmä (esim. HIV-infektion seurauksena), sillä et / lapsesi ei välttämättä saa Prevenar 20 -rokotuksesta täyttä hyötyä.
Keskustele lääkärin, apteekkihenkilökunnan tai sairaanhoitajan kanssa ennen rokotusta, jos lapsesi on hyvin pieni keskonen (syntynyt raskausviikolla 28 tai ennen sitä), sillä hengitys voi hidastua 2–3 päiväksi rokotuksen jälkeen.
Kuten kaikkien muidenkin rokotteiden kohdalla, Prevenar 20 ei suojaa kaikkia rokotteen saaneita.
Prevenar 20 suojaa vain tiettyjen Streptococcus pneumoniae ‑bakteerityyppien aiheuttamilta korvatulehduksilta, sillä se on kehitetty vain niitä vastaan. Se ei suojaa muilta korvatulehduksia mahdollisesti aiheuttavilta taudinaiheuttajilta.
Muut lääkevalmisteet/rokotteet ja Prevenar 20
Prevenar 20 -rokote voidaan antaa lapselle samaan aikaan muiden tavanomaisten lapsuusiässä annettavien rokotteiden kanssa.
Aikuisille Prevenar 20 -rokote voidaan antaa samanaikaisesti (inaktivoidun) influenssarokotteen kanssa eri pistoskohtiin. Terveydenhuollon ammattilaisen tekemän yksilöllisen riskiarvion mukaan voi olla suositeltavaa antaa nämä rokotteet erikseen, esimerkiksi 4 viikon välein.
Aikuisille Prevenar 20 -rokote voidaan antaa samaan aikaan COVID-19-mRNA-rokotteen kanssa.
Kerro lääkärille, apteekkihenkilökunnalle tai sairaanhoitajalle, jos parhaillaan otat tai lapsesi parhaillaan ottaa, olet äskettäin ottanut tai lapsesi on äskettäin ottanut, tai saatat ottaa tai lapsesi saattaa ottaa muita lääkkeitä tai jos olet tai lapsesi on äskettäin saanut jonkin toisen rokotuksen.
Raskaus ja imetys
Jos olet raskaana tai imetät, epäilet olevasi raskaana tai jos suunnittelet lapsen hankkimista, kysy lääkäriltä tai apteekista neuvoa ennen tämän rokotteen ottamista.
Ajaminen ja koneiden käyttö
Prevenar 20 -valmisteella ei ole haitallista vaikutusta ajokykyyn ja koneidenkäyttökykyyn. Jotkut kohdassa Mahdolliset haittavaikutukset ”Mahdolliset haittavaikutukset” mainitut vaikutukset voivat kuitenkin vaikuttaa tilapäisesti ajokykyyn tai koneidenkäyttökykyyn.
Prevenar 20 sisältää natriumia
Tämä lääkevalmiste sisältää alle 1 mmol natriumia (23 mg) per annos eli sen voidaan sanoa olevan ”natriumiton”.
3. Miten valmistetta käytetään
Lääkäri tai sairaanhoitaja injisoi suositellun rokoteannoksen (0,5 ml) olkavartesi tai lapsen olkavarren tai reiden lihakseen.
Imeväiset (ikä 6 viikkoa – 15 kuukautta)
Lapsi saa kolmesta pistoksesta koostuvan perusrokotussarjan ja sen jälkeen tehosteannoksen.
- Ensimmäinen pistos voidaan antaa jo 6 viikon iässä ja 8 viikon ikään asti.
- Jokainen pistos annetaan siten, että välissä on vähintään 4 viikkoa, lukuun ottamatta viimeistä pistosta (tehosteannos), joka annetaan 11–15 kuukauden iässä.
Sinulle kerrotaan, milloin lapsi on tuotava vastaanotolle seuraavaa pistosta varten.
Kysy lisätietoja lääkäriltä, apteekkihenkilökunnalta tai sairaanhoitajalta maasi virallisisten suositusten mukaisesta rokotusohjelmasta.
Keskoset (syntyneet ennen raskausviikkoa 37)
Lapsi saa kolmesta pistoksesta koostuvan perusrokotussarjan ja sen jälkeen tehosteannoksen. Ensimmäinen pistos voidaan antaa jo 6 viikon iässä siten, että annosten väli on vähintään 4 viikkoa. Lapsi saa neljännen pistoksen (tehosteannos) 11–15 kuukauden iässä.
Rokottamattomat imeväiset (ikä 7 kuukautta – 11 kuukautta)
Imeväisille (ikä 7 kuukautta – 11 kuukautta) annetaan kolme pistosta. Kaksi ensimmäistä pistosta annetaan vähintään 4 viikon välein. Kolmas pistos annetaan toisena ikävuotena.
Rokottamattomat lapset (ikä 12 kuukautta – 23 kuukautta)
Lapsille (ikä 12 kuukautta – 23 kuukautta) annetaan kaksi pistosta vähintään 8 viikon välein.
Rokottamattomat lapset (ikä 2–4 vuotta)
Lapsille (ikä 2–4 vuotta) annetaan yksi pistos.
Prevenar 13 ‑rokotteella aiemmin rokotetut lapset (ikä 15 kuukautta – 4 vuotta)
Lapset (ikä 15 kuukautta – 4 vuotta), jotka ovat aiemmin saaneet Prevenar 13 ‑rokotuksen, saavat yhden pistoksen.
Lapset ja nuoret (ikä 5–17 vuotta) riippumatta siitä, ovatko he aiemmin saaneet Prevenar 13 -rokotuksen
Lapset ja nuoret (ikä 5–17 vuotta) saavat yhden pistoksen.
Jos lapsi on saanut aiemmin Prevenar 13 ‑rokotteen, on odotettava vähintään 8 viikkoa, ennen kuin Prevenar 20 annetaan.
Aikuiset
Aikuiset saavat yhden pistoksen.
Jos olet aiemmin saanut pneumokokkirokotuksen, kerro siitä lääkärille, apteekkihenkilökunnalle tai sairaanhoitajalle.
Jos sinulla on kysymyksiä Prevenar 20 -rokotteen käytöstä, käänny lääkärin, apteekkihenkilökunnan tai sairaanhoitajan puoleen.
Erityisryhmät
Henkilöt, joilla katsotaan olevan tavanomaista suurempi pneumokokki-infektion riski (esim. joilla on sirppisolutauti tai HIV-infektio), mukaan lukien 23-valenttisella pneumokokkipolysakkaridirokotteella rokotuksen aiemmin saaneet, voivat saada vähintään yhden Prevenar 20 -annoksen.
Henkilöt, jotka ovat saaneet kantasolusiirron, voivat saada kolme pistosta, joista ensimmäinen annetaan 3–6 kuukautta siirron jälkeen ja joiden välillä on oltava vähintään 4 viikkoa. Neljännen pistoksen (tehosteannos) antamista 6 kuukauden kuluttua kolmannesta pistoksesta suositellaan.
4. Mahdolliset haittavaikutukset
Kuten kaikki rokotteet, Prevenar 20 -rokotekin voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa.
Prevenar 20 -rokotteen vakavat haittavaikutukset
Kerro heti lääkärille, jos huomaat jonkin seuraavista vakavien haittavaikutusten oireista (ks. myös kohta Mitä sinun on tiedettävä ennen valmisteen käyttöä): kasvojen, huulten, suun, kielen tai kurkun turvotus (edeema), hengenahdistus (dyspnea), hengityksen vinkuminen (bronkospasmi) – nämä voivat olla merkkejä vakavasta allergisesta reaktiosta, kuten anafylaksia, mukaan lukien sokki.
Muut haittavaikutukset
Seuraavia haittavaikutuksia on raportoitu annettaessa Prevenar 20 -rokotetta imeväisille ja lapsille (ikä 6 viikkoa – 4 vuotta):
Hyvin yleinen: voi ilmetä useamman kuin 1 rokoteannoksen yhteydessä 10:stä
- heikentynyt ruokahalu
- ärtyisyys
- unisuuden tunne
- kuume
- kaikilla lapsilla pistoskohdassa: punoitus, kovettuma tai turvotus, kipu tai aristus
- 2 – < 5-vuotiailla lapsilla ja tehosteannoksen jälkeen pistoskohdassa: punoitus, yli 2,0–7,0 cm:n laajuinen kovettuma tai turvotus.
Yleinen: voi ilmetä enintään 1 rokoteannoksen yhteydessä 10:stä
- ripuli
- oksentelu
- ihottuma
- kuume (38,9 °C:n tai korkeampi kuume)
- pistoskohdassa perusrokotussarjan jälkeen: punoitus, yli 2,0–7,0 cm:n laajuinen kovettuma tai turvotus, liikkumiseen vaikuttava kipu tai aristus.
Melko harvinainen: voi ilmetä enintään 1 rokoteannoksen yhteydessä 100:sta
- kouristuskohtaukset, mukaan lukien kuumeen aiheuttamat
- nokkosihottuma (urtikaria tai urtikarian kaltainen ihottuma)
- pistoskohdassa: punoitus, yli 7,0 cm:n laajuinen kovettuma tai turvotus.
Harvinainen: voi ilmetä enintään 1 rokoteannoksen yhteydessä 1 000:sta
- pistoskohdan allerginen reaktio (yliherkkyysreaktio).
Seuraavia haittavaikutuksia on raportoitu Prevenar 13 ‑rokotteen käytössä ja niitä voidaan havaita myös Prevenar 20 -rokotteen käytössä:
- pyörtyminen tai sokin kaltainen tila (hypotonis-hyporesponsiivinen episodi)
- allerginen reaktio (yliherkkyysreaktio), mukaan lukien kasvojen ja/tai huulten turvotus
- itkuisuus
- levoton uni.
Seuraavia haittavaikutuksia on raportoitu Prevenar 20 -rokotteen käytössä lapsilla ja nuorilla (5–17 vuotta):
Hyvin yleinen: voi ilmetä useamman kuin 1 rokoteannoksen yhteydessä 10:stä
- päänsärky
- lihaskipu
- pistoskohdassa: kipu, aristus, punoitus, kovettuma tai turvotus
- väsymys.
Yleinen: voi ilmetä enintään 1 rokoteannoksen yhteydessä 10:stä
- nivelkipu
- pistoskohdassa: liikkumiseen vaikuttava kipu tai aristus.
Melko harvinainen: voi ilmetä enintään 1 rokoteannoksen yhteydessä 100:sta
- nokkosihottuma (urtikaria tai urtikarian kaltainen ihottuma)
- kuume.
Seuraavia haittavaikutuksia on raportoitu Prevenar 13 ‑rokotteen käytössä ja niitä voidaan havaita myös Prevenar 20 -rokotteen käytössä:
- ripuli
- oksentelu
- heikentynyt ruokahalu
- ärtyisyys
- unisuuden tunne
- levoton uni
- ihottuma.
Lapsilla ja nuorilla, joilla on joko HIV-infektio tai sirppisolutauti tai jotka ovat saaneet verta muodostavan kantasolusiirron, haittavaikutukset ovat olleet samankaltaisia, mutta oksentelun, ripulin, kuumeen, nivelkivun ja injektiopaikassa esiintyvän liikkumiseen vaikuttavan kivun tai arkuuden esiintyvyys on ollut hyvin yleistä.
Seuraavia haittavaikutuksia on raportoitu myyntiluvan myöntämisen jälkeen lapsilla Prevenar 13 ‑rokotteen käytössä ja niitä voidaan havaita myös Prevenar 20 -rokotteen käytössä:
- vaikeat allergiset reaktiot, mukaan lukien sokki (kardiovaskulaarinen kollapsi), huulten, kasvojen tai kurkun turpoaminen (angioedeema)
- suurentuneet imusolmukkeet (lymfadenopatia) rokotuskohdan läheisyydessä, kuten kainaloissa tai nivusissa
- pistoskohdassa: nokkosihottuma (urtikaria), punoitus ja ärsytys (dermatiitti) sekä kutina.
- punaläiskäinen, kutiava ihottuma (erythema multiforme).
Seuraavia haittavaikutuksia on raportoitu Prevenar 20 -rokotteen käytössä aikuisilla:
Hyvin yleinen: voi ilmetä useamman kuin 1 rokoteannoksen yhteydessä 10:stä
- päänsärky
- nivelkipu ja lihaskipu
- pistoskohdan kipu/aristus sekä väsymys.
Yleinen: voi ilmetä enintään 1 rokoteannoksen yhteydessä 10:stä
- pistoskohdan turvotus, pistoskohdan punoitus sekä kuume.
Melko harvinainen: voi ilmetä enintään 1 rokoteannoksen yhteydessä 100:sta
- ripuli, pahoinvointi ja oksentelu
- ihottuma sekä kasvojen, huulten, suun, kielen tai nielun turpoaminen, mistä voi aiheutua nielemis- tai hengitysvaikeuksia (angioedeema)
- pistoskohdan kutina, turvonneet imusolmukkeet kaulassa, kainaloissa tai nivusissa (lymfadenopatia), nokkosihottuma pistoskohdassa (urtikaria) ja vilunväristykset.
Seuraavia haittavaikutuksia on havaittu Prevenar 13 ‑rokotteen käytössä ja niitä voidaan havaita myös Prevenar 20 -rokotteen käytössä:
- punaläiskäinen, kutiava ihottuma (erythema multiforme)
- pistoskohdan ärsytys
- heikentynyt ruokahalu
- käsivarren liikerajoitus.
Haittavaikutuksista ilmoittaminen
Jos havaitset haittavaikutuksia, kerro niistä lääkärille, apteekkihenkilökunnalle tai sairaanhoitajalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Voit ilmoittaa haittavaikutuksista myös suoraan (ks. yhteystiedot alla). Ilmoittamalla haittavaikutuksista voit auttaa saamaan enemmän tietoa tämän lääkevalmisteen turvallisuudesta.
www‐sivusto: www.fimea.fi
Lääkealan turvallisuus‐ ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
00034 FIMEA
5. Valmisteen säilyttäminen
Ei lasten ulottuville eikä näkyville.
Älä käytä tätä lääkettä ulkopakkauksessa ja etiketissä mainitun viimeisen käyttöpäivämäärän EXP jälkeen. Viimeinen käyttöpäivämäärä tarkoittaa kuukauden viimeistä päivää.
Säilytä jääkaapissa (2 °C–8 °C).
Prevenar 20 pitää käyttää mahdollisimman pian jääkaapista ottamisen jälkeen.
Ei saa jäätyä. Hävitä rokote, jos se on jäätynyt.
Säilyvyystiedot osoittavat rokotteen säilyvyydeksi 96 tuntia 8–25 °C:n lämpötilassa säilytettynä tai 72 tuntia 0–2 °C:n lämpötilassa säilytettynä. Prevenar 20 on näiden ajanjaksojen päättyessä käytettävä tai hävitettävä. Nämä tiedot on tarkoitettu terveydenhuollon ammattilaisille ohjeellisiksi vain tilapäisten lämpötilapoikkeamien yhteydessä.
Esitäytetyt ruiskut pitää säilyttää jääkaapissa vaakatasossa suspension uudelleensekoittamiseen kuluvan ajan minimoimiseksi.
Lääkkeitä ei pidä heittää viemäriin eikä hävittää talousjätteiden mukana. Kysy käyttämättömien lääkkeiden hävittämisestä apteekista. Näin menetellen suojelet luontoa.
6. Pakkauksen sisältö ja muuta tietoa
Mitä Prevenar 20 sisältää
Vaikuttavat aineet ovat seuraavia CRM197-kantajaproteiiniin konjugoituja polysakkarideja:
- 2,2 mikrogrammaa serotyyppien 1, 3, 4, 5, 6A, 7F, 8, 9V, 10A, 11A, 12F, 14, 15B, 18C, 19A, 19F, 22F, 23F ja 33F polysakkaridia
- 4,4 mikrogrammaa serotyypin 6B polysakkaridia.
Yksi annos (0,5 ml) sisältää noin 51 mikrogrammaa CRM197-kantajaproteiinia adsorboituna alumiinifosfaattiin (0,125 mg alumiinia).
Muut aineet ovat natriumkloridi, meripihkahappo, polysorbaatti 80 ja injektionesteisiin käytettävä vesi.
Lääkevalmisteen kuvaus ja pakkauskoko (-koot)
Rokote on valkoinen injektioneste, suspensio, kerta-annoksen sisältävässä esitäytetyssä ruiskussa (0,5 ml). Saatavana ovat pakkauskoot 1, 10 ja 50 ruiskua, joissa on neulat tai ei ole neuloja. Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
Myyntiluvan haltija ja valmistaja
Myyntiluvan haltija: Pfizer Europe MA EEIG Boulevard de la Plaine 17 1050 Bruxelles Belgia | Erän vapauttamisesta vastaava valmistaja: Pfizer Manufacturing Belgium NV Rijksweg 12 2870 Puurs-Sint-Amands Belgia |
Lisätietoja tästä lääkevalmisteesta antaa myyntiluvan haltijan paikallinen edustaja:
Suomi/Finland
Pfizer Oy
Puh/Tel: +358 (0)9 430 040
Tämä pakkausseloste on tarkistettu viimeksi 03/2024.
Muut tiedonlähteet
Lisätietoa tästä lääkevalmisteesta on saatavilla Euroopan lääkeviraston verkkosivulla http://www.ema.europa.eu .
Ohjeet terveydenhuollon ammattilaiselle
Säilytyksen aikana voidaan havaita valkoista sakkaa ja pinnalla kirkas liuos. Tämä ei ole laadun heikkenemisen merkki. Esitäytetyt ruiskut pitää säilyttää vaakatasossa suspension uudelleensekoittamiseen kuluvan ajan minimoimiseksi.
Käyttöön valmistelu
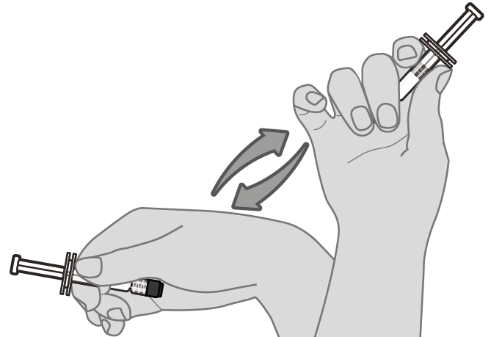
| Vaihe 1. Rokotteen uudelleensekoittaminen suspensioksi Pidä esitäytettyä ruiskua peukalon ja etusormen välissä vaakatasossa ja ravista voimakkaasti, kunnes ruiskun sisältö on homogeeninen valkoinen suspensio. Älä käytä rokotetta, jos se ei sekoitu suspensioksi. |
 |
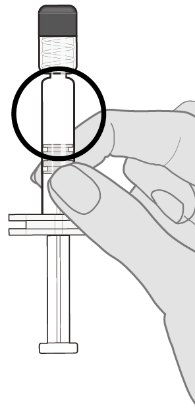
| Vaihe 2. Silmämääräinen tarkistus Tarkista rokote silmämääräisesti ennen antoa, ettei siinä ole suuria hiukkasia eikä värimuutosta. Älä käytä, jos havaitset suuria hiukkasia tai värimuutoksen. Jos rokote ei ole homogeeninen valkoinen suspensio, toista vaiheet 1 ja 2. |
 |
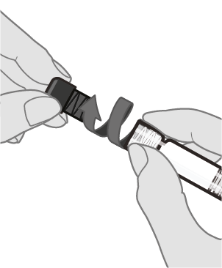
| Vaihe 3. Irrota ruiskun korkki Irrota ruiskun korkki Luer lock ‑liittimestä kiertämällä korkkia hitaasti vastapäivään. Pidä samalla kiinni Luer lock ‑liittimestä. Huom.: Ruiskun korkkia irrotettaessa on varottava tarkoin painamasta ulos vedettynä olevaa männän vartta. |
 |
| Vaihe 4. Kiinnitä steriili neula Kiinnitä esitäytettyyn ruiskuun lihakseen antoon soveltuva neula pitämällä kiinni Luer lock ‑liittimestä ja kiertämällä neulaa myötäpäivään. |
Anna koko annos.
Prevenar 20 on tarkoitettu annettavaksi vain lihakseen.
Prevenar 20 -rokotetta ei saa sekoittaa muiden rokotteiden tai lääkevalmisteiden kanssa samassa ruiskussa.
Prevenar 20 -rokotetta voidaan antaa samaan aikaan muiden lapsuusiän rokotteiden kanssa, mutta silloin on käytettävä eri rokotuskohtia.
Prevenar 20 -rokote voidaan antaa aikuisille samanaikaisesti kausi-influenssarokotteen (nelivalenttinen influenssarokote [QIV]; pinta-antigeeni, inaktivoitu, sisältää adjuvanttia) kanssa. Henkilöille, joilla on perussairauksia, joihin liittyy suuri hengenvaarallisen pneumokokkitaudin kehittymisen riski, voidaan harkita QIV-rokotteen ja Prevenar 20 -rokotteen antamista erikseen (esim. noin 4 viikon välein). Rokotteet on pistettävä eri kohtiin.
Prevenar 20 -rokote voidaan antaa aikuisille samaan aikaan COVID‑19-mRNA-rokotteen (nukleosidimuokattu) kanssa.
Käyttämätön lääkevalmiste tai jäte on hävitettävä paikallisten vaatimusten mukaisesti.